问题
计算题
某气态烃A和B按2︰3(体积比)混合后,取0.1mol与一定量氧气混合燃烧,产物为CO、CO2和水蒸气。将燃烧产物依次通过足量的浓硫酸、灼热的CuO及碱石灰,最后碱石灰增重7.04g。求A和B可能的分子式
答案
A的分子式为CH4,B的分子式可能为C2H6、C2H4、C2H2。
(1)碱石灰吸收的CO2包括燃烧生成的CO2及CO转化(还原CuO)成的CO2,即0.1mol混合烃中的C转化成CO2的总量,共为7.04g÷44g/mol="0.16mol"
可知:1mol混合烃含碳1.6mol,所以混合烃一定含CH4
(2)设另一烃分子中含x个碳原子
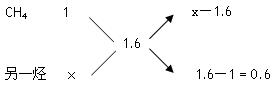
(1)令A为CH4,则有
(x—1.6)/ 0.6 = 2/3,解得x=2
B可能是C2H6、C2H4、C2H2。
(2)令B为CH4,则有
0.6 /(x—1.6)=2/3,解得x=2.5(不合理,舍去)。
以此得A的分子式为CH4,B的分子式可能为C2H6、C2H4、C2H2。
