实验室用下列有关装置先制取干燥、纯净的Cl2并进行漂白性性质实验,试根据下列装置回答有关问题.
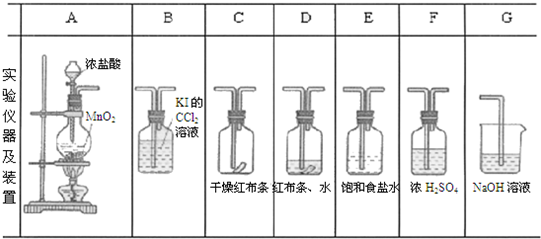
(1)上述装置中各仪器从左至右的连接顺序是______.
(2)E装置目的是______,D装置是为了______,
(3)分别写出A、G中的化学反应原理______.
(1)实验室用A装置制备氯气,经过除杂干燥后分别通入C、D装置中进行漂白性性质实验,然后通入到B中验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用G装置吸收氯气,故答案为:A、E、F、C、D、B、G;
(2)因饱和食盐水中含有大量的Cl-,对Cl2的溶解有抑制作用,使Cl2+H2O
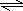
H++Cl-+HClO平衡向左移动,故可用饱和食盐水除去HCl.氯气与水反应产生盐酸和次氯酸,次氯酸具有漂白性,可使用色布条褪色,但干燥氯气不能使有色布条褪色,二者为对比参照实验,
故答案为:除去HCl;做对比参照实验;
(3)A为制备氯气的发生装置,二氧化锰与浓盐酸在加热条件反应生成氯气、氯化锰和水,该反应的化学方程式为
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,G为尾气处理装置,氯气与NaOH反应生成氯化钠和次氯酸钠,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O, △ .
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;Cl2+2NaOH=NaCl+NaClO+H2O. △ .
