某兴趣小组在实验室用铜和硫酸为原料多种方法制取硫酸铜.制备方法如下:
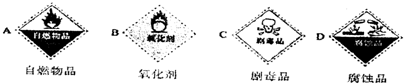
方法一:铜与浓硫酸反应(1)浓硫酸试剂瓶上适合贴上的标签是______(可多选 ).
(2)甲同学取6.4g铜片和10mL 18mol•L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色固体.甲同学为了验证其中白色固体的主要成分.设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌.
实验现象:______;实验结论:所得白色固体的化学式为______.
(3)甲还观察到加热时,在试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失.淡黄色固体消失的原因是(用化学反应方程式回答)______.
方法二:
(4)乙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2
2CuO,CuO+H2SO4=CuSO4+H2O.对比甲的方案,你认为乙同学设计的实验方案的优点是______. △ .
方法三:
(5)丙同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色.写出反应的化学反应方程式______.
方法四:
(6)请你再帮助该实验小组的同学设计一种只用铜和稀硫酸为原料制取硫酸铜的方法,写出该方法中的化学反应方程式:______.
(1)因浓硫酸具有强烈的腐蚀性、强氧化性,则选择的标签为BD,故答案为:BD;
(2)灰白色的固体中加入适量蒸馏水,若观察到溶液为蓝色,则所得白色固体为CuSO4,故答案为:溶液为蓝色;CuSO4;
(3)试管内壁上部析出少量淡黄色固体物质,由存在的元素可知淡黄色固体物质为S,S具有还原性,浓硫酸具有强氧化性,
S与浓硫酸发生氧化还原反应为S+2H2SO4(浓)
3SO2↑+2H2O,而使淡黄色物质消失,故答案为:S+2H2SO4(浓) △ .
3SO2↑+2H2O; △ .
(4)由2Cu+O2
2CuO,CuO+H2SO4=CuSO4+H2O可知,不生成有毒气体二氧化硫,则其优点为不产生有毒气体污染环境,故答案为:生成物对环境无污染; △ .
(5)铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色,是发生了氧化还原反应所致,该反应为Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;
(6)Cu与稀硫酸不反应,若只用铜和稀硫酸为原料制取硫酸铜,则可设计为电解池,让Cu作阳极,硫酸作电解质溶液,反应为Cu+H2SO4
CuSO4+H2↑, 电解 .
故答案为:Cu+H2SO4
CuSO4+H2↑. 电解 .
