为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验.
实验步骤如下:先分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.按图示连接好仪器,点燃蜡烛,同时从a导管口抽气.一段时间后熄灭蜡烛,再分别称量蜡烛、装置Ⅱ、装置Ⅲ的质量.实验数据如表.
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为______.(相对原子质量:H一1;C-12;O-16)
(3)装置Ⅱ和装置Ⅲ的顺序能否颠倒?______(填“能”或“不能”).
(4)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是______.
(5)该实验能否准确测出蜡烛燃烧生成二氧化碳和水的质量?______(填“能”或“不能”),理由是______.
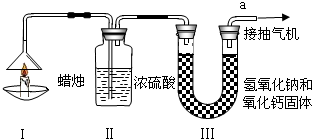
(1)分析表格,装置二盛放的是浓硫酸,吸收的是水,原来质量是182.3g,后来是184.1g,所以生成水的质量是:184.1g-182.3g=1.8g,装置三盛放的是氢氧化钠溶液,吸收的是二氧化碳,原来质量是212.2g,后来是216.6g,所以生成二氧化碳的质量是:216.6g-212.2g=4.4g,所以本题答案为:1.8g;4.4g;
(2)1.8g水含氢元素的质量为:1.8g×
=0.2g,4.4g二氧化碳含碳元素的质量为:4.4g×2 18
=1.2g,所以碳氢元素的质量比为:1.2g:0.2g=6:1;12 44
(3)若两装置换位置,则导致水与氧化钙反应,导致测得的水的质量不准确,所以本题答案为:不能;
(4)根据质量守恒定律,参加反应的各物质的质量和等于生成的各物质的质量和,消耗的蜡烛+氧气=水+二氧化碳,所以装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,所以本题答案为:生成的二氧化碳和水的总质量为蜡烛失去的质量和氧气的质量总和;
(5)要准确测出蜡烛燃烧生成二氧化碳和水的质量,需要排除空气中原有的二氧化碳和水,而本题的装置中没有除水和除二氧化碳的装置,故测定的结果不准确,所以本题答案为:不能;未除去空气中本来就有的二氧化碳和水.
