有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.
(1)检验矿物样品中是否有Fe3+
实验用品:锤子、研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
实验步骤:
①取样:将样品用锤子敲碎,再在研钵中研细备用.
②溶将样品粉末倒入烧杯,加入______,用玻璃棒充分搅拌.
③______(填操作名称).
④检验:取少许溶液,______.
实验现象:______.
实验结论:矿物样品中含有Fe3+.
(2)制备氢氧化亚铁
①为了得到亚铁盐的溶液,同学们在剩余的溶液中加入过量的某种固体试剂,该试剂是(填化学式)______,反应的离子方程式是______.
②对于①中过量的固体试剂是否需要除去,同学们产生了两种观点.
甲组:认为需要过滤. 乙组:认为不需要过滤.
你支持的是组______(填“甲”或“乙”),理由是______
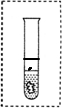
③同学们在新制得的亚铁盐溶液中加入适量新制的氢氧化钠溶液,制出的氢氧化亚铁呈______色.为使试管中的氢氧化亚铁保存的时间更长,请在右图中画出你的设计(可以加必要的文字说明).

(1)氧化铁可以和盐酸反应生成氯化铁和水,将氯化铁和难溶物质分离的方法可以采用过滤法,三价铁遇到硫氰酸钾显示红色,可以用硫氰酸钾检验三价铁离子的存在,
故答案为:稀盐酸;过滤; 滴加KSCN溶液;溶液变为红色;
(2)①金属铁可以和三价铁之间发生反应生成亚铁离子,为了得到亚铁盐的溶液,可以在剩余的氯化铁溶液中加入过量的铁,发生反应:2Fe3++Fe=3Fe2+,
故答案为:Fe;2Fe3++Fe=3Fe2+;
②在氯化铁和金属铁反应生成氯化亚铁的反应中,过量的铁不必除去,因为亚铁离子很容以被氧化为三价铁,为了防止被氧化,需加入金属铁,
故答案为:乙;过量的铁粉可以防止Fe2+被氧化为Fe3+;
③氢氧化亚铁易被空气中的氧气氧化为氢氧化铁,为了防止被氧化,必须隔绝氢氧化亚铁和空气的接触,可覆盖一层和水互不相溶且密度小于水的液体乳:植物油、苯等,
故答案为:白;
.
