问题
问答题
结合如图所示的实验装置(铁架台等辅助仪器略去未画)
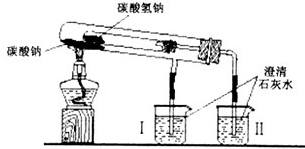
回答下列问题:
(1)在加热过程中能观察到产生白色沉淀的烧杯是______(填“Ⅰ”、“Ⅱ”)烧杯.该烧杯中发生反应的离子方程式是:______,通过实验甲可比较出Na2CO3、NaHCO3两种固体,______更稳定.
(2)若某Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法为______;若某NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的化学方程式为______.
答案
(1)在加热过程中,碳酸氢钠受热分解生成二氧化碳,二氧化碳与澄清石灰水变浑浊,所以烧杯Ⅱ中出现白色沉淀,反应的离子方程式为:Ca2++CO2+2OH-=CaCO3↓+H2O,通过该实验证明了碳酸钠稳定性大于碳酸氢钠,
故答案为:Ⅱ;Ca2++CO2+2OH-=CaCO3↓+H2O;Na2CO3;
(2)若某Na2CO3固体中混有少量NaHCO3杂质,可以通过加热方法使碳酸氢钠分解生成碳酸钠而除去;若某NaHCO3溶液中混有少量Na2CO3杂质,可以通入二氧化碳气体,使碳酸钠与二氧化碳反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3,
故答案为:加热;Na2CO3+CO2+H2O=2NaHCO3.
