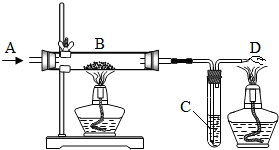
利用如图装置可进行气体性质的探究实验.A处通入无色气体(可能是H2、CO或CO2);B处玻璃管中盛放黑色粉末(可能是CuO或C),C处试管中盛放澄清石灰水.
①根据要求完成下表填写:
| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象:______. |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式:______, 发生氧化反应的物质是:______. |
| Ⅲ | 若为CO2与C的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有______色的火焰. |
③探究实验Ⅱ澄清石灰水的作用(用发生反应的化学方程式表示)______.
④在上述探究实验Ⅱ、Ⅲ中,D处导管尖嘴口都需用酒精灯点燃,简述其目的分别是:______、______.
①氢气还原氧化铜生成铜,故黑色氧化铜变成红色的铜;一氧化碳与氧化铜反应生成铜和二氧化碳,一氧化碳发生的氧化反应;二氧化碳与碳在高温条件下发生反应生成一氧化碳,一氧化碳点燃产生蓝色火焰;
②无水硫酸铜遇水会变成蓝色,这是检验反应有无水生成的一个重要手段;
③二氧化碳能使澄清石灰水变浑浊,澄清石灰水是检验有无二氧化碳生成的常用方法;
④酒精灯点燃的作用是:实验Ⅱ目的是除去有毒的CO尾气,防止污染;实验Ⅲ主要目的是证明高温下CO2与C能反应,且产物为CO.
故答案为:①黑色粉末变成红色;CO+CuO
Cu+CO2;CO;蓝.②位置:在B、C之间或C之前;药品:白色无水硫酸铜.③Ca(OH)2+CO2═CaCO3↓+H2O.④实验Ⅱ目的是除去有毒的CO尾气,防止污染;实验Ⅲ主要目的是证明高温下CO2与C能反应,且产物为CO.△ .
