现有药品:Wg(W<1)锌片、稀硫酸、无水硫酸铜、氧化铜和水.请从图中选用适当实验装置,设计一个最简单的实验,粗略地测定锌原子量(假定环境为标准状况).
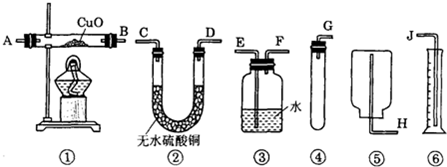
(1)应选用的装置是(只要求写出图中装置的标号)______.
(2)所用装置的连接顺序是(填各接口的字母,连接胶管省略)______.
(3)操作中,怎样加放试剂以保证不漏出氢气?______.
(4)用实验所测得的数据,写出计算锌原子量的数学式:______,锌的原子量=______.
(1)从提供的药品可以看出求锌的相对原子质量的关系建立在锌与硫酸的反应,并对生成的氢气的体积进行测量,进而可求出氢气的质量,利用化学方程式可求锌的原子量,该设计选择装置,图中④是制取氢气的装置,③是收集氢气并排水的装置,⑥是测量排出水的体积.故答案为:③④⑥
(2)制取氢气的装置在前,利用③装置排水时应是气体由短管通入,水由长管排出,用⑥测量出排出水的体积进而确定收集到的氢气的体积.故答案为:G→F→E→J
(3)操作中,为了保证不漏出氢气,则注意加放试剂:向试管中加入足量的稀硫酸后,将试管斜放,再把锌片放在试管内壁上,塞紧塞子,将试管慢慢直立,让锌片滑下与硫酸接触发生反应.
(4)水的体积即是生成氢气的体积换算出氢气的质量,利用化学方程式进行计算可求出锌的原子量.由题意知:氢气的质量为:2
.V(H2) 22.4
设锌的相对原子质量为x
Zn+H2SO4=ZnSO4+H2↑
x2
Wg 2
gV(H2) 22.4
则
=x wg
,解得x=2 2
gV(H2) 22.4
,而锌的原子量=65.22.4W V(H2)
故答案为:(1)③④⑥.
(2)G→F→E→J.
(3)向试管中加入足量的稀硫酸后,将试管斜放,再把锌片放在试管内壁上,塞紧塞子,将试管慢慢直立,让锌片滑下与硫酸接触发生反应.
(4)
,65.22.4W V(H2)
