问题
问答题
(1)12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是______,
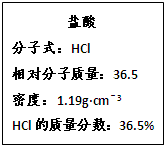
(2)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试回答下列问题:
①该浓盐酸中HCl的物质的量浓度为______.
②若用KMnO4氧化上述盐酸.其反应方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
当有1molKMnO4恰好和盐酸全部完全反应,反应后溶液的体积为2L,则所得溶液中Cl-的物质的量浓度为______,此时产生的Cl2在标准状况下的体积为______.
答案
(1)12.4gNa2X中含Na+0.4mol,则Na2X摩尔质量为0.2mol,其摩尔质量=
=62g/mol,12.4g 0.2mol
故答案为:62g/mol;
(2)①由c=
可知,该浓盐酸中HCl的物质的量浓度=1000ρw M
mol/L=11.9mol/L,1000×1.19×36.5% 36.5
故答案为:11.9mol/L;
②1molKMnO4恰好和盐酸全部完全反应,则:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
1mol 1mol 1mol 2.5mol
则反应后溶液中Cl-的浓度=
=1.5mol/L,1mol+1mol×2 2L
生成氢气的体积为2.5mol×22.4L/mol=56L,
故答案为:1.5mol/L;56L.
