问题
计算题
(6分)
Na2CO3与盐酸反应分两步进行:
第一步反应为:Na2CO3+HCl===NaCl+NaHCO3;
第二步反应为:NaHCO3+HCl===NaCl+H2O+CO2↑
取Na2CO3溶液100g,逐滴加入稀盐酸直到过量。反应过程中产生的气体质量与加入
的盐酸质量的关系如图所示:

(1)反应中最多可以产生CO2___________g。
(2)求Na2CO3溶液中溶质质量分数(要求书写计算过程)。
(相对原子质量:C—12、Na—23、H—1、O—16)
答案
(1)4.4 (2)10.6g%
题目分析:(1)根据图像可知,生成二氧化碳的质量最多为4.4g;
(2)根据题意可知:反应为碳酸钠与盐酸反应生成二氧化碳气体、氯化钠和水;已知量为二氧化碳的质量4.4g;未知量为溶液中碳酸钠的质量分数。解题思路:可根据反应中二氧化碳与碳酸钠的质量关系计算出碳酸钠的质量,再进一步求解碳酸钠溶液中溶质的质量分数。具体过程如下:
解:设含碳酸钠的质量为x
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 44
x 4.4g
106:44=x:4.4g
x=10.6g
溶液中碳酸钠的质量分数为: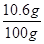 ×100%=10.6g%
×100%=10.6g%
答:碳酸钠溶液中溶质的质量分数为10.6g%
