问题
填空题
为了测定某饱和卤代烃的分子中卤原子的种类和数目,可按下列步骤进行实验: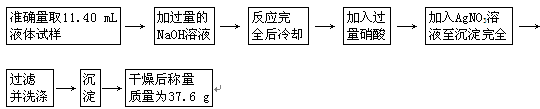 回答下列问题:
回答下列问题:
(1)准确量取11.40 mL液体所用仪器是________;
(2)加入过量硝酸的作用是___________________________________________;
(3)加入AgNO3溶液时产生的沉淀为浅黄色,则此卤代烃中的卤原子是________;
(4)已知此卤代烃液体的密度是1.65 g/mL,其蒸气对甲烷的相对密度是11.75,则此卤代烃每个分子中卤原子的数目为_______个;此卤代烃的结构简式为: _。
答案
1)酸式滴定管(1分) (2)中和过量的NaOH(1分)
(3)溴原子(1分) (4)2(2分) CH2BrCH2Br、CH3CHBr2(写2个给2分)
题目分析:因加入AgNO3溶液时产生的沉淀为浅黄色,故卤代烃中卤原子为溴。
溴代烃的质量为11.40 mL×1.65 g/mL=18.8 g,且相对分子质量为16×11.75=188,
因此溴代烃的物质的量为 。
。
而n(AgBr)= =0.2 mol,故每个卤代烃分子中溴原子数目为2。
=0.2 mol,故每个卤代烃分子中溴原子数目为2。
根据相对分子质量判断其结构简式可能为 或CH3CHBr2。
或CH3CHBr2。
点评:测定物质的结构简式是有机化学中的常考知识点,难度不大,主要综合考查学生的实验操作能力、计算能力,解题的关键是根据实验的步骤,逐步推断。
