气体的制取和性质等一系列问题的研究历来是中学化学的重要内容.
I.有下列仪器装置、实验示意图
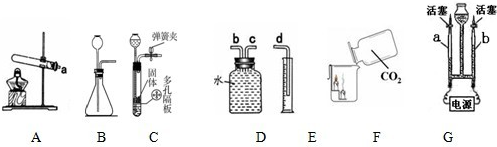
(1)写出实验室制取CO2 的化学方程式______
(2)B和C装置均可制CO2,其中用C装置的优点是______
(3)实验F体现二氧化碳具有的性质有______
(4)用A作气体发生装置制氧气,通过排水量测定所收集到的氧气体积,装置的连接顺序是:a→b→c→d,请在图上画出装置内导管(“b”或“c”)该怎样延伸.
(5)通过电解水的方法也可以得到氧气(上图装置G).
①检验b玻璃管(碱式滴定管)内气体的方法是什么?②此探究实验的目的是什么?
Ⅱ、(1)质量相同的下 * * 种物质,完全分解后制得氧气质量最多的是______.
A.过氧化氢 B.高锰酸钾 C.氯酸钾 D.水 E.氧化汞
(2)从(1)中A~E任选一种物质制取6.4g氧气,请通过化学方程式计算消耗该物质的质量.
I.(1)实验室用大理石和稀盐酸反应制取CO2,反应的化学方程式CaCO3+2HCl═CaCl2 +H2 O+CO2 ↑;
(2)C装置的优点是可随时控制反应的发生与停止;
(3)实验F的现象是下层的蜡烛先熄灭,上层的蜡烛后熄灭,体现二氧化碳不能燃烧,也不支持燃烧,密度比空气大;
(4)若各装置的连接顺序是:a→b→c→d,F装置内导管应c管延长,有利于排水,故如图

;
(5)①b玻璃管(碱式滴定管)内气体是氧气,氧气的检验方法是打开活塞,用带火星的木条放在玻璃管尖嘴口;②此探究实验的目的是探究水的组成;
Ⅱ、(1)可设生成的氧气都为32g,则有
2H2O2
2H2O+O2↑; MnO2 .
68 32
2KMnO4
K2MnO4 +MnO2 +O2↑; △ .
316 32
KClO32 3 MnO2 . △
KCl+O2↑;2 3
81.7 32
2H2O
2H2↑+O2 ↑; 通电 .
36 32
2HgO
2Hg+O2↑ △ .
433 32
比较可知生成相同质量的氧气,水用的最少,反之等质量的五种物质制氧气,完全反应后生成氧气最多的是水.
故选D;
(2)选过氧化氢,设制取6.4g氧气,消耗过氧化氢的质量为x.
2H2O2
2H2O+O2↑ MnO2 .
68 32
x 6.4 g
=68 32
,解得x=13.6gx 6.4g
故答案为:
I、(1)CaCO3+2HCl═CaCl2 +H2 O+CO2 ↑;
(2)可随时控制反应的发生与停止;
(3)二氧化碳不能燃烧,也不支持燃烧,密度比空气大;
(4)

;
(5)①打开活塞,用带火星的木条放在玻璃管尖嘴口;②探究水的组成;
II、(1)D;
(2)选过氧化氢,设制取6.4g氧气,消耗过氧化氢的质量为13.6g.