问题
选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.7.8g Na2O2含有的阴离子数目为0.2NA
B.0.5mol雄黄(As4S4,结构如图
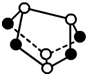
)含有5NA个S-S键
C.14g乙烯和丙烯(C3H6)的混合物中含有的原子数目为3NA
D.常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA
答案
A、Na2O2含有O22-离子,7.8g Na2O2的物质的量是0.1mol,所以7.8g Na2O2含有的阴离子物质的量是0.1mol,数目为0.1NA,故A错误.
B、一个雄黄分子中含有2个S-S键,0.5mol雄黄中含有1molS-S键,所以含有NA个S-S键,故B错误.
C、乙烯和丙烯最简式相同,14g由乙烯和丙烯最简式CH2的物质的量为1mol,含有原子数为3NA,故C正确.
D、常温下,铁和浓硝酸发生钝化现象导致铁不能完全溶解,所以转移电子数小于,故D错误.
故选C.
