问题
实验题
(1)下面是教材下册中“物质溶解时的吸热或放热现象”的活动与探究。请你一同完成该探究并回答有关问题:
| 水中加入的溶质 | NaCl固体 | NH4NO3固体 | NaOH固体 |
| 加溶质前水的温度/℃ | 20 | 20 | 20 |
| 溶解现象 | 全部溶解 | 全部溶解 | 全部溶解 |
| 溶质溶解后溶液的温度变化 | 温度无明显变化 | 温度降低 | 温度升高 |
| 结论(“放热”或“吸热”) | 固体氯化钠溶于水无明显放热和吸热现象 | ① | ② |
(2)下图“→”表示A在一定条件下可以转化为B,“—”表示相连的两种物质间在一定条件下可以发生反应。A、B、C、D各是一氧化碳、木炭粉、氧化铜、氧气中的某一种物质,请你推断(用化学式表示):
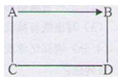
B是 ,D是 。
答案
①吸热②放热③>(2)CO CuO
解:(1)硝酸铵溶解于水温度降低,所以可以知道硝酸铵溶解时表现出来的是吸收热量,同时说明NH4NO3固体溶解时扩散过程吸收的热量大于水合过程放出的热量;而氢氧化钠溶于水温度升高,所以氢氧化钠表现出来的是放出热量;
(2)根据C和D分别可以和两种物质发生反应,所以可以知道C和D分别为氧气、氧化铜或者一氧化碳,但是A能够生成B,所以可以判断A为碳单质,那么B为就是一氧化碳,所以C为氧气,而D为氧化铜;
故答案为:(1)①吸热;
②放热;
③>;
(2)CO;CuO.

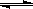 2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是
2C(g)+D(g)中,各物质的平均反应速率间的关系式正确的是