生活中用到各种漂白剂。化学课上,老师带来一种常用作氧系漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠(2Na2CO3·3H2O2)和过氧化钙(CaO2)中的一种。同学们观察发现,该漂白剂为白色粉末(右图)。

【提出猜想】该漂白剂肯定不是 。
【查阅资料】①过碳酸钠是一种白色结晶颗粒,溶于水时,分解生成碳酸钠
和过氧化氢。
②过氧化氢常温下不稳定,实验室用过氧化氢制取氧气的化学方程式为 。
③过氧化钙,白色固体,难溶于水。与水反应缓慢释放氧气,同时生成一种碱,反应的化学方程式为 。
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整。
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 取2g白色固体放入试管中,加入5ml水,充分振荡。 | 液体浑浊, 有持续的细小气泡冒出。 | |
| 步骤2 | 向步骤1的试管中继续滴加无色酚酞。 | 无色酚酞变红。 | |
| 步骤3 | 。 | 。 | 该消毒剂的成分不是过碳酸钠。 |
实验现象2分,其他每空1分,其他合理答案得分
提出猜想:H2O2
查阅资料:②2H2O2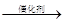 2H2O + O2↑
2H2O + O2↑
③ 2CaO2 + 2H2O = 2Ca(OH)2 + O2↑
实验验证:操作——向试管中滴加稀盐酸,将产生的气体通入澄清石灰水
现象——溶液红色消失,有气泡产生,澄清石灰水不变浑浊
交流反思:小刚:溶液浑浊,说明该漂白剂难溶于水,而过氧化钙难溶于水,过碳酸钠能溶于水,说明该漂白剂是过氧化钙
小强:一定量的水中固体不完全溶解,可能是因为固体不溶,也可能是因为水量不足,溶解达到饱和,所以不能确定是过氧化钙。
分析:【提出猜想】根据双氧水是液态进行分析;
【查阅资料】②根据实验室过氧化氢制氧气的原理进行分析;
③根据题中的叙述找出反应物、生成物书写方程式;
【实验验证】根据结论分析添加的试剂和发生的现象进行分析;
【交流反思】根据过氧化钙、过碳酸钠和水会生成气体进行分析.
解答:解:【提出猜想】该漂白剂为白色粉末,而双氧水是液态的,所以不是双氧水,故答案为:双氧水;
【查阅资料】②双氧水在二氧化锰的催化作用下生成水和氧气,故答案为:2H2O2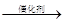 2H2 O+O2↑;
2H2 O+O2↑;
根据质量守恒定律可知该碱是氢氧化钙,过氧化钙和水反应会生成氢氧化钙和氧气,故答案为:2CaO2+2H2O═2Ca(OH)2+O2↑;
【实验验证】从结论中可以看出该步骤检验的是碳酸钠,检验碳酸盐常加入酸,
| 实验步骤 | 实验操作 | 实验现象 | 实验结论 |
| 步骤1 | 取2g白色固体放入试管中,加入5mL水,充分振荡. | 液体浑浊,有持续的细小气泡冒出. | |
| 步骤2 | 向步骤1的试管中继续滴加无色酚酞. | 无色酚酞变红. | |
| 步骤3 | 继续滴加稀盐酸 | 无气泡产生,酚酞红色褪去 | 该漂白剂的成分不是过碳酸钠. |
水的量较少,也不会将碳酸钠全部溶解,故答案为:过碳酸钠与水反应也有气体产生,且生成的碳酸钠可能不能完全溶解在5mL水中.
