(10分)某同学设计了测定空气中氧气含量的实验,实验装置如图。该同学的实验步骤如下:
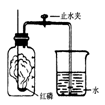
①将图中的集气瓶分为5等份,并作好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是 。
(2)步骤③中打开止水夹后观察到的现象是 _____
____________________________,由此可得出空气中氧气的体积分数约为 。
(3)该实验可推论出氮气__________(填“易”或“难”)溶于水和其化学性质________(填“活泼”或“不活泼”)的结论。
(4)若将红磷换成炭粉,该实验能否获得成功?为什么?
(1)使集气瓶中的氧气完全消耗
(2)烧杯内的水沿导管流入集气瓶中,液面大约在标记1处 1/5(或21%)
(3)难不活泼
(4)否,碳燃烧生成二氧化碳气体,使瓶内气压变化不大,水不能进入瓶内
解答:解:(1)该实验中红磷需稍过量,目的是把瓶内的氧气全部耗尽,以得出正确的实验结论.故答案为:充分反应掉集气瓶中的氧气
(2)红磷与氧气反应,生成了白烟--五氧化二磷.故答案为:发出黄光,产生热量,生成了大量的白烟;水沿导管被吸入集气瓶中,大约占瓶内容积的五分之一;20%
(3)水进入瓶内占五分之一.说明氮气不能与红磷反应,也不能溶于水或与水反应、故答案为:难;不活泼
(4)炭粉尽管能与氧气反应,除去了瓶内的氧气,但由于反应生成了二氧化碳气体,因此瓶内的气体没有减少,气压不会减小,故实验不能测定出空气中氧气的含量.故答案为:不能成功;因为碳燃烧产生气体,使瓶中大气压不变
