(9分)某课外活动小组在学习了铜与氧气反应(2Cu+O2=2CuO)这一性质后,想做一做“空气中氧气含量的测定”实验,并在最后将铜丝进行回收。
(1)课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50 mL空气,如图。然后给装有铜丝的玻璃管加热。同时交替推动两个注射器的活塞,至玻璃管内的铜丝变黑且较长时间内无进一步变化时停止。停止加热后,待冷却至室温将气体全部推至一个注射器内。
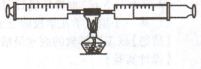
请根据你对上述实验的理解,回答下列问题:
①实验结束后,注射器内空气的体积减少了约 mL,这是因为
②在实验的加热过程中,交替缓慢推动两个注射器的目的是 。
③上述实验只是粗略测定空气中氧气含量的一种方法,你认为造成该实验不够精确的
可能原因是 。
(2)课外活动小组发现红热的铜丝变黑后,为了回收再利用铜丝,在研究如何除去黑色
物质的讨论中,制定了下列方案。

请根据以上方案回答:
① 乙方案的烧杯中发生反应的化学方程式为
两种方案相比较,甲方案的不足之处是 。
②若采用甲、乙两种方案处理此变成黑色的铜丝,并且充分反应,则回收的铜丝a的质
量 (填“<”、“>”、“=”)铜丝b的质量。
(9分)(1) ①10 空气中氧气体积约占 1/5 . (各1分)② 让铜充分与氧气反应;(1分)③铜丝未能完全消耗掉注射器内的氧气或装置漏气;(2分)
(2)① CuO + 2HCl ="=" CuCl2 + H2O; (1分) CO有毒,尾气CO未处理,实验装置复杂等。(2分)② > (1分)
:(1)由于铜的氧化反应只消耗掉了空气中的氧气,而氧气在空气中约占空气体积的
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
(2)①碱性氧化物与酸反应生成盐和水可写出化学方程式:CuO+2HCl=CuCl2+H2O;从实验操作与环境保护方面看用乙方案要好些,故答案为:乙;甲方案使用CO,操作不便,浪费能源,而且可能对环境造成污染
②解:两种方案一种是用一氧化碳还原氧化铜,另一种是用盐酸去除表面的氧化铜,从两种方案的反应原理可知铜丝a的质量要大于铜丝b的质量.
实验消耗氧气的质量:0.01L×1.3g/L=0.013g
设被0.013g氧气氧化的铜的质量为x
2Cu+O2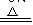 2CuO
2CuO
2×64 32
x 0.013g
2×64:32= x:0.013g
x=0.05g,这0.05g铜最终进入了溶液,所以b最后剩余的铜就少了0.05g
答案为:a铜丝质量>b铜丝质量,理论上a铜丝比b铜丝多0.05g
