(2011年浙江舟山,30题)科学探究是科学研究与学习的一种重要方式。
请完成下列有关探究技能的问题。
(1)找证据:收集、分析各种证据是认识物质的基本方法。如汗液有咸味,因此有同学认
为汗液中有氯化钠。为了验证猜想,他收集了一定量的汗液,然后向其中滴加一种化学试剂,
看到有白色沉淀生成,这种化学试剂是 。
(2)推理:食盐和工业用盐(主要成分为亚硝酸钠,化学式NaNO2)都有咸味,但亚硝酸
钠对人体是有剧毒的。比较食盐和亚硝酸钠的化学式,可推断亚硝酸钠组成成分中的
是有剧毒的。(用化学符号表示)
(3)处理数据:在测定硫酸铜晶体结晶水质量分数的实验中,得到的数据如表:(已知坩埚质量为8.7克)则该实验测得硫酸铜晶体中结晶水的质量分数为 。
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 坩埚和硫酸铜晶体总质量(g) | 10.7 | 10.1 | 9.8 | 9.8 | 9.8 |
AgNO3溶液 NO2- 45%
析:(1)可根据汗液的成分结合课本知识进行分析.
(2)可对比二者的化学式的组成的共同和不同进行分析.
(3)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.结合图示数据和化学方程式进行分析.
解答:解:(1)汗液中含有代谢产物氯化钠及一些油脂,用AgNO3溶液与汗液可发生反应 AgNO3+NaCl═AgCl↓+NaNO3
故答案为:硝酸银溶液
(2)对比二者化学式可知都含有共同的钠离子,所以其作用的例子肯定是亚硝酸根离子,
故答案为:NO2-
(3)解:根据图示可知硫酸铜晶体的质量=第一次坩埚+试剂的质量-坩埚质量=10.7g-8.7g=2.0g.
由图示数据可知,第三次、第四次和第五次的质量相等.说明硫酸铜晶体中的水分已被蒸发干,
故无水硫酸铜的质量=9.8g-8.7g=1.1g.
所以结晶水的质量=硫酸铜晶体的质量-无水硫酸铜的质量=2.0g-1.1g=0.9g.
所以结晶水的含量= × 100%=
× 100%=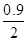 ×100%=45%
×100%=45%
故答案为:45%
