某活动小组根据下图所示进行模拟炼铁的实验,并对产物的成分进行探究。
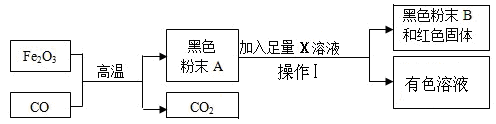
【提出问题】黑色粉末A可能是什么呢?
【查阅资料】小华查阅资料,得到关于铁的氧化物如下信息:
| 铁的氧化物 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 物理性质 | 不能被磁铁吸引 | 能被磁铁吸引 | 不能被磁铁吸引 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸,但不生成气体 |
【提出猜想】(1)小明认为黑色粉末A全部是铁粉。为了证明自己的猜想小明设计了如上图的实验,该实验中,小明加入的X溶液是 ;实验过程中操作Ⅰ是 这个实验基本操作。
小华根据小明的实验认定小明的猜想是错误的,理由是 。
(2)小华根据资料提出了自己的两个猜想,请结合所学知识补充余下的一个猜想。
猜想①:黑色粉末A由铁粉和四氧化三铁(Fe3O4)组成
猜想②:黑色粉末A由铁粉和氧化亚铁(FeO)组成
猜想③:
【实验探究】
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 取适量黑色粉末A 用磁铁吸引 | 猜想①正确 | |
| ② | 适量黑色粉末A 用磁铁吸引 | 黑色粉末部分被吸引 | 猜想②正确 |
| ③ | 猜想③正确 |
【反思评价】小娟认为方案②中得出的结论不正确,其理由是 。
【得出结论】黑色粉末A是铁和氧化亚铁的混合物。
小华想测定黑色粉末A中铁的质量分数,设计了如下实验:
取8g黑色粉末A加入50g足量的稀硫酸,充分反应后称量,剩余物质的质量为57.8g,则该黑色粉末A中铁的质量分数是多少?(写出计算过程)
(1)硫酸铜溶液、过滤;加入足量硫酸铜溶液反应后过滤,还有黑色粉末存在
(2)猜想3:黑色粉末A由铁粉、氧化亚铁和四氧化三铁组成
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 黑色粉末A全部被吸引 | ||
| ② | |||
| ③ | 取适量黑色粉末B,加入足量稀盐酸 (或者取适量黑色粉末B用磁铁吸引;黑色粉末部分被吸引) | 黑色粉末B部分溶解 (黑色粉末B部分被吸引) |
【反思评价】:含有四氧化三铁时,也发生同样的现象
计算:略,算出铁的质量1分,算出质量分数1分
:(1)由黑色粉末A加入足量X溶液得到有色溶液和黑色固体、红色固体,常见的红色固体是铜,根据置换反应可知铁把铜置换出来了,所以加入的溶液是铜的盐溶液,可认为是硫酸铜溶液,硫酸铜与铁反应能生成铜和硫酸亚铁,硫酸亚铁是浅绿色的;把不溶于液体的固体与液体分离的方法是过滤;由于加入的硫酸铜是足量的,所以固体中的铁都能被反应掉,通过检测发现加入硫酸铜后,还有黑色固体不溶物,说明不可能全部为铁,小明认为黑色粉末A全部是铁粉,所以该说法错误;
(2)黑色粉末有:铁粉、四氧化三铁(Fe3O4)、氧化亚铁,所以这三种相互组合情况有:黑色粉末A由铁粉和四氧化三铁(Fe3O4)组成、黑色粉末A由铁粉和氧化亚铁(FeO)组成、黑色粉末A由铁粉、氧化亚铁和四氧化三铁组成;因为铁粉能被磁铁吸引,四氧化三铁也能被磁铁吸引,所以如果是这两种物质组成,现象为:黑色粉末A全部被吸引;由于氧化亚铁溶于酸,四氧化三铁不溶于酸,所以加入酸,看黑色固体是否被溶解,如果部分溶解,说明含有四氧化三铁;小娟认为方案②中得出的结论不正确她认为含有四氧化三铁时,也发生同样的现象;
根据质量的减少量是生成氢气的质量,所以生成氢气的质量为:8g+50g-57.8g=0.2g,设要生成0.2g氢气,需要铁质量为X则:Fe+H2SO4=FeSO4+H2↑
56 2
X 0.2g
根据: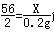 解得X=5.6g,则该黑色粉末A中铁的质量分数是
解得X=5.6g,则该黑色粉末A中铁的质量分数是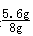 ×100%=70%.
×100%=70%.
故答案为:(1)硫酸铜溶液、过滤;加入足量硫酸铜溶液反应后过滤,还有黑色粉末存在
(2)猜想3:黑色粉末A由铁粉、氧化亚铁和四氧化三铁组成
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 黑色粉末A全部被吸引 | ||
| ② | |||
| ③ | 取适量黑色粉末B,加入足量稀盐酸 (或者取适量黑色粉末B用磁铁吸引;黑色粉末部分被吸引) | 黑色粉末B部分溶解 (黑色粉末B部分被吸引) |
计算:70%
