(2010•义乌市)2010年5月12日,在苍茫海水中沉没了800多年的“南海一号”重见天日,其中的宋代铜钱已经锈迹斑斑.已知:铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它受热分解的化学方程式为:Cu2(OH)2CO3 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
某同学设计了如下实验,用来测定碱式碳酸铜受热分解后产生的水和二氧化碳的质量比.
实验用到的主要装置为:

(1)装置连接顺序为: .(填写编号)
(2)操作步骤及数据处理:
第一步 检查气密性;
第二步 装入药品,称取装置①和③的质量;
第三步 试验后再次称取装置①和③的质量,记录数据如表;
| 质 装置 量 时间 | 装置① | 装置③ |
| 实验前 | 220.0克 | 195.0克 |
| 实验后 | 222.1克 | 199.4克 |
(3)结果分析;从下列选项中选出产生该实验结果可能的原因有哪些? .
A.二氧化碳没有被完全吸收 B.水没有被完全吸收
C.碱式碳酸铜药品中含有水分 D.碱式碳酸铜没有完全分解.
(1)②→①→③(或②①③)(2)21:44(3)AC
题目分析:(1)要测定分解生成的水和二氧化碳的质量,需要先使碱式碳酸铜受热分解,然后使分解的产物先通过浓硫酸吸收水分,测定水的质量,然后使产物通过氢氧化钠溶液,测定二氧化碳的质量,故填:②→①→③(或②①③);
(2)根据实验数据可知,生成的水的质量为:222.1g﹣220.0g=2.1g,生成的二氧化碳的质量为:199.4g﹣195.0g=4.4g,所以水和二氧化碳的质量比为:2.1g:4.4g=21:44,故填:
21:44;
(3)Cu2(OH)2CO3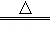 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
44 18
根据反应的化学方程式可知,生成的水和二氧化碳的质量比为18:44,而测定的结果是比值大于理论的结果,则可能是二氧化碳吸收不完全,或碱式碳酸铜样品中含有水分,
A、二氧化碳没有被完全吸收,导致二氧化碳的质量变小,使测定结果的比值大于理论值,正确;
B、水没有被完全吸收,不会使测定结果的比值大于理论值,错误;
C、碱式碳酸铜药品中含有水分,会使水的质量变大,使测定结果的比值大于理论值,正确;
D、碱式碳酸铜没有完全分解,不会影响水与二氧化碳的比值,错误;
观察选项,故填:AC.
点评:本题考查了常见物质分解成分的质量关系,完成此题,可以依据题干提供的信息结合已有的知识进行
