(10广东省23)同学们在学碱的化学性质时,做了一个如下图所示的甲乙两个实验。
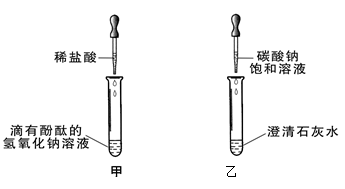
(1)写出乙实验的化学反应方程式______________________________,反应过程中产生的现象是________________________________。
实验结束后,甲、乙两个同学将废液倒入实验室的废液缸,结果发现废液浑浊并呈红色,产生疑问。
【提出问题】 废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和_______(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是_______________。(写一种猜想)
【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。

【反思拓展】 在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑________。
(1)Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
澄清石灰水变浑浊(或产生白色沉淀)
【交流讨论】①氯化钠
②NaOH [或NaOH、Ca(OH)2]
【实验设计】

【反思拓展】反应物的用量
碳酸钠和澄清的石灰水反应生成碳酸钙沉淀,和氢氧化钠。反应的化学方程式为Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH,① NaOH + HCl= NaCl + H2O 所以废液中含有碳酸钙、指示剂、水和氯化钠,②有白色沉淀生成,溶液呈红色,证明废液中有碳酸钠和氢氧化钠,小林的猜想正确,有白色沉淀,溶液呈无色说明废液中有碳酸钠,小云的猜想正确,无白色沉淀,溶液呈红色,说明废液中只有氢氧化钠,小红的猜想正确。【反思拓展】除了考虑生成物外还需考虑反应物的过量,
