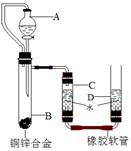
(9分)小黄用右图装置测定铜锌合金中锌的质量分数和锌的相对原子质量。主要实验步骤如下(必要的固定装置已略去):
①连接装置并检查装置气密性;
②加入药品和水;
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加试剂至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中液面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥将B中剩余固体过滤、洗涤、干燥并称重,称得剩余固体质量为W g。
(1)A仪器的名称为 ▲ ;
(2)B中发生的反应的化学方程式为: ▲ ;
(3)小黄在实验前将块状的铜锌合金磨成粉末状,其目的是: ▲ ;
(4)如何检验该装置的气密性: ▲ ;
(5)为使测得的气体体积更精确,记录C中液面刻度时,除使视线与凹液面的最低处相平外,还应 ▲ ;
(6)小黄发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是: ▲ ;
(7)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验: ▲ ;理由是 ▲ 。
(9分)
(1)分液漏斗(1分) (2)Zn+H2SO4==ZnSO4+H2↑(2分)
(3)加快反应的速率(1分)
(4)提高D管,静止片刻后,C、D液面仍存在高度差,则气密性良好(答案合理即1分)
(5)使D、C中的液面相平(1分)
(6)测量铜锌合金样品的质量(1分)
(7)重新实验(1分)中途添加酸时,会造成气体逸散,影响气体体积的精确测量(1分)
(1)熟记常用的一些仪器名称;
(2)根据反应物和生成物,书写化学方程式Zn+2HCl═ZnCl2+H2↑
(3)铜锌合金磨成粉末状,其目的是:接触面积大,充分反应;目的为了提高反应速率;
(4)注意检验该装置的气密性的方法:提高D管,静止片刻后,C、D液面仍存在高度差,则气密性良好;
(5)除使视线与凹液面的最低处相平外,还应D处观察上升的是否与C中下降的一致;
(6)已知气体的体积,根据密度,可以求出气体的质量;又知道剩余固体质量为Wg,但不知道原固体的质量,无法计算.实验中由于数据缺乏而无法计算,该步骤是:测量铜锌合金的总质量;
(7)中途添加酸时,会造成气体逸散,影响气体体积的精确测量,所以要重新实验.
故答案为:
(1)分液漏斗;
(2)Zn+2HCl═ZnCl2+H2↑
(3)加快反应的速率
(4)提高D管,静止片刻后,C、D液面仍存在高度差,则气密性良好(答案合理即可)
(5)使D、C中的液面相平
(6)测量铜锌合金样品的质量
(7)重新实验;中途添加酸时,会造成气体逸散,影响气体体积的精确测量
点评:题主要考查了金属的化学性质和一些实验的操作注意事项,掌握检验该装置的气密性的方法,了解量气的装置.
