问题
实验题
请参与某学习小组进行研究性学习的过程,并协助完成相关任务:
[提出问题] 在平时探讨酸的性质时,我们通常是讨论酸的水溶液。究竟水在酸显示酸的特性时扮演什么角色呢?
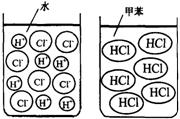
[确定研究对象] 以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究。[查阅资料] 氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如下图)。
[设计与实验] (请完成下表)
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的的甲苯溶液: A | 氯化氢的甲苯溶液中没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液: B | 化学方程式: C |
| 氯化氢的甲苯溶液:没有明显的现象 | 氯化氢在甲苯溶液中没有解离出氢离子 | |
| 与固体碳酸钠的作用 | 氯化氢的水溶液:产生气泡 | 化学方程式: D |
| 氯化氢的甲苯溶液: | 氯化氢在甲苯中没有解离出氢离子 |
答案
A不导电;B 固体溶解,产生无色气泡;C.Mg+2HCl=MgCl2+H2
D.Na2CO3+2HCl=2NaCl+H2O+CO2 E.H+
某些物质溶于水时能电离出自由移动的离子,这些阴阳离子都带电荷,而使溶液能导电,酸类物质具有相似的化学性质是由于它们的溶液中都含有H+,本题就欲说明溶液中若无H+,即使是在水溶液中表现出较强酸性的HCl分子,因不含H+也不具有酸类物质的通性.
