双休日后,小丽带着快乐的心情返回学校。当她来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液,由此,激发了她的探究欲望。
《提出问题》这瓶NaOH溶液一定变质了,其变质程度如何呢?
《提出猜想》小丽的猜想:NaOH溶液部分变质
你的新猜想: 。
《实验探究》小丽设计如下实验来验证自己的猜想,请根据表中内容填写小丽实验时的现象:
假设你的猜想正确,并按小丽的实验方案进行实验,则你观察到的实验现象是
。
《实验反思》下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH) 2溶液、④Ba(OH)2
溶液,能替代小丽实验中CaCl2溶液的是 (填序号)。
《拓展应用》小丽想测定这瓶变质的NaOH溶液中Na2CO3的质量分数。现取20g待测溶液,向其中逐滴加入CaCl2溶液,产生沉淀质量与所加CaCl2物质的量的关系如图所示。
(1)B点处所得溶液中溶质有 。
(2)求待测溶液中Na2CO3的质量分数。
( 写出计算过程)
氢氧化钠溶液全部(或完全)变质
产生白色沉淀,酚酞变红色
只产生白色沉淀,酚酞不变色
①、②
(1)NaCl、Na2CO3、NaOH(全对给1分)
(2)设样品中含Na2CO3为Xmol
Na2CO3 + CaCl2→2NaCl + CaCO3↓ ………………………(1分)
1mol 1mol
Xmol 0.01mol
X=0.01mol ………………………………………(1分)
Na2CO3质量分数=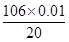 ×100%= 5.3% ……………… (1分)
×100%= 5.3% ……………… (1分)
【提出猜想】NaOH溶液全部变质
【实验探究】氢氧化钠在空气中会与空气中的二氧化碳反应生成碳酸钠,检验氢氧化钠是否全部变质,也就是看碳酸钠中还有没有剩余的氢氧化钠.通过检验碳酸根离子和氢氧根离子的方法可以确定.故答案为:产生白色沉淀,溶液变红
产生白色沉淀,溶液不变红
【实验反思】若用氢氧化钡或氢氧化钙的话,即使原溶液中没有氢氧化钠反应也会生成氢氧化钠.故答案为①②
【拓展应用】
(1)当氯化钙溶液滴加到B点时,碳酸钠没有反应完,还有生成的氯化钠,原溶液中可能还有未变质的氢氧化钠.故答案为:NaOH、NaCl、Na2CO3或NaCl、Na2CO3
(2)解:设Na2CO3的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111
x 100g×1.11%=1.11g

答:待测溶液中碳酸钠的质量分数为5.3%.
