(8分)化学小组的同学对碳燃烧产生兴趣。
提出问题:将3克碳与8克氧气放入密闭容器中燃烧,产物只有二氧化碳吗?
猜想与假设:燃烧后气体一定含有CO2,可能含有 。
查阅资料:向氯化钯(PdCl2) 溶液中通入CO,发生下列反应。请完成化学方程式的书写PdCl2+CO+H2O==Pd↓黑色+CO2+2 。
设计实验:小刚设计了下图所示装置。 结合图示回答问题:
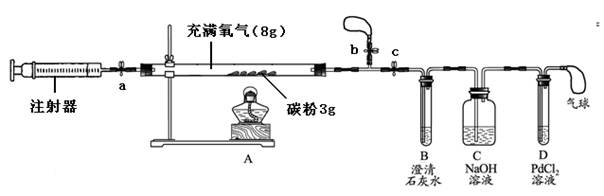 实验步骤:
实验步骤:
(1)打开弹簧夹a,关闭弹簧夹b、c 。点燃酒精灯,加热碳粉,A装置中观察到的现象是 。
(2)过一会儿,打开弹簧夹b,推动注射器的活塞。
(3)打开弹簧夹c,用注射器向装置中缓缓注入氮气,观察到B中澄清石灰水变浑浊,反应的化学方程式为 。小组同学通过实验确定有一氧化碳生成,他们依据的现象是 。
实验结论:综合上述实验,并进行理论推导,得出结论。3g碳在8g氧气中燃烧后的混合物中含有 。
实验反思:在整个实验过程中,注射器的作用有 。
(8分)
猜想与假设:CO、O2
查阅资料:HCl
实验步骤:(1)碳剧烈燃烧,发白光
(3)CO2+Ca(OH)2=CaCO3↓+H2O ,D中有黑色沉淀产生
实验结论:CO2、CO 、O2
实验反思(2分,答出任意一点得1分,答全得2分):减小A装置中容器压强;补充氧气;推动反应后气体进入BCD装置
猜想与假设:根据质量守恒定律,3克碳与8克氧气如果恰好完全反应,只生成二氧化碳;如果碳不充分燃烧就会生成一氧化碳,并且氧气有剩余;因此燃烧后气体一定含有CO2,可能含有一氧化碳和氧气,故答案为:CO、O2
查阅资料:根据质量守恒定律:反应前后原子的种类和数目不变,可以判断生成物是氢氯酸,故答案为:HCl
实验步骤:(1)加热碳粉,A装置中观察到的现象是:碳剧烈燃烧,发白光.故答案为:碳剧烈燃烧,发白光
(3)二氧化碳和石灰水反应生成碳酸钙白色沉淀和水,D中有黑色沉淀产生,故答案为:CO2+Ca(OH)2=CaCO3↓+H2O,D中有黑色沉淀产生
实验结论:根据实验现象来判断生成物的组成是CO2、CO、O2,故答案为:CO2、CO、O2
实验反思:注射器的作用有:减小A装置中容器压强;补充氧气;推动反应后气体进入BCD装置等;故答案为:减小A装置中容器压强;补充氧气;推动反应后气体进入BCD装置
