某研究型学习小组的同学在用浓硫酸测定废锌片中锌的纯度时,没有将浓硫酸稀释直接处理废锌片发现产生的气体具有刺激性气味(废锌片中其它杂质不与硫酸反应),这种现象引起同学们的思考和研究。
【提出猜想】对产生的气体进行猜想:
猜想1:只有H2;
猜想2:只有SO2;
猜想3:可能是
小华认为不需做实验根据已有知识就可知道猜想1是错误的,他的依据是 。
【资料】①浓硫酸有强氧化性,其与活泼金属反应不生成氢气,② SO2能使品红溶液褪色
【实验方案】研究性学习小组的同学设计下图所示的装置进行研究(夹持仪器已省略,假设装置中的反应都进行完全)。
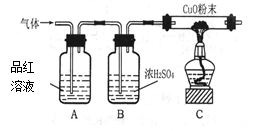
根据实验现象小组得到共同结论是猜想3成立。
(1) 他们的实验现象是
装置B中浓硫酸的作用是 (2)小华对实验结果产生疑问:
你认为小华产生疑问的依据是
你认为猜想3成立可能原因是:
【拓展应用】
(1)稀硫酸与锌反应能产生氢气(Zn+H2SO4=ZnS04+H2 ↑),而浓硫酸与锌反应开始时不产生氢气(Zn+(浓)2H2SO4=ZnS04+SO2↑+2 ),
由此可知反应物相同,但 不同生成物也不同。
(2)取废锌片8g(废锌片中其它杂质不与硫酸反应)加入足量浓硫酸至固体质量不再减少为止,过滤,将滤液蒸干共得晶体16.1g,此废锌片的纯度是 。
(3)如果用浓硫酸来直接测定废锌片中锌的纯度时,尾气必须处理,可将尾气通入足量的石灰水里其反应方程式是 。
【提出猜想】 H2和SO2 , 氢气没有刺激性气味
(1)【实验方案】他们的实验现象是A中品红溶液褪色C中黑色固体变成红色
装置B中浓硫酸的作用是 干燥进入C中的气体 (2)你认为小华产生疑问的依据是 浓硫酸有强氧化性,其与活泼金属反应
不生成氢气
你认为可能原因是: 反应过程中消耗硫酸浓硫酸逐渐变成稀硫酸
【思维拓展】(1) H2O , 浓度 。
(2) 81.25% 。
(3) Ca(OH)2+SO2=CaSO3↓+ H2O 。
【提出猜想】因为闻到有刺激性气味,而氢气没有刺激性气味,所以不可能就是氢气一种。
【实验方案】SO2能使品红溶液褪色,氢气能还原氧化铜,所以二者都有的话实验现象为A中品红溶液褪色C中黑色固体变成红色,浓硫酸有吸水性,所以可以干燥进入C中的气体。
(2)因为由资料可知浓硫酸有强氧化性,其与活泼金属反应不生成氢气,但是随着反应,浓硫酸会变成稀硫酸。
【思维拓展】(1)根据反应前后原子的种类和个数不变既可以得出。因为稀硫酸产生氢气,而浓硫酸生成的是水,所以反应物的浓度不同生成物也不同。
(2)得到的晶体16.1g为硫酸锌,所以可以根据化学方程式通过生成16.1克硫酸锌求出锌的质量为6.5克,所以此废锌片的纯度是6.5/8=81.25%
(3)二氧化硫与石灰水反应方程式为Ca(OH)2+SO2=CaSO3↓+ H2O
