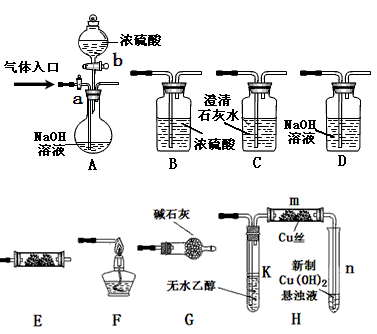
造成酸雨的主要物质是二氧化硫(SO2),某兴趣小组的同学收集某地刚降到地面的雨水进行实验.
【相关信息】①用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
| 测定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| PH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
【分析讨论】①酸雨能使土壤酸化,农业上常用 中和酸性土壤.
②酸雨能腐蚀金属制品,请写出一种防止室外金属被腐蚀的方法 .
③收集的酸雨样品放置一段时间后pH减小,原因是SO2与H2O反应生成H2SO3被氧化为H2SO4,请写出H2SO3被氧化生成H2SO4的化学方程式 .
【提出猜想】同学们对收集到的酸雨样品的溶质进行猜想:
猜想I:酸雨中溶质为H2SO3
猜想II:酸雨中溶质为H2SO4
猜想III:酸雨中溶质为
【实验探究】向收集的酸雨样品中滴加过量的Ba(OH)2溶液,有白色沉淀生成,过滤,向沉淀中加入足量的稀盐酸,请完成下表:
| 现象 | 结论 |
| ①如果沉淀没有溶解 | 则猜想 正确 |
| ②如果沉淀全部溶解,并放出有刺激性气味的气体 | 则猜想 正确 |
| ③如果 | 则猜想III正确 |
【分析讨论】①氢氧化钙;
②涂油漆(涂油、保持金属表面干燥等);
③2H2SO3+O2═2H2SO4;
【提出猜想】既有H2SO3又有H2SO4;I;II;沉淀部分溶解且放出有刺激性气味气体;BaSO3+2HCl=BaCl2+SO2↑+H2O;
【拓展延伸】NO3﹣
【分析讨论】①农业上治理酸化土壤的方法是采用氢氧化钙与土壤中的酸发生中和反应,从而降低酸性;
②金属生锈的条件是水与氧气共存,所以防止金属生锈的方法即是控制生锈的条件,常用的方法有涂油漆、涂油、保持金属表面干燥等;
③H2SO3被氧化为H2SO4的方程式为:2H2SO3+O2═2H2SO4;
【提出猜想】综合猜想I、II两种情况分析可知猜想III应该是两者都有;
从反应的现象推断猜想的合理性,①如果沉淀没有溶解,因为硫酸钡不溶于酸,所以可判断溶液中只含有硫酸;
②如果沉淀全部溶解,并放出有刺激性气味的气体,说明溶液中不含有硫酸,只含有亚硫酸;
③从何①②可知猜想III成立则应该是既有不溶的沉淀又有可溶的沉淀,且溶解时放出有刺激性气味的气体;
④依据稀盐酸加入后沉淀溶解并放出有刺激性气味气体,可知该反应是亚硫酸钡和盐酸,生成物是氯化钡、二氧化硫和水,其方程式为:BaSO3+2HCl=BaCl2+SO2↑+H2O;
【拓展延伸】因为形成酸雨的气体主要是二氧化硫及二氧化氮所以酸雨中除去含有以上酸根外,还可能含有硝酸根