(6分)利用干燥而纯净的氢气还原氧化铜的实验测定水的质量组成,装置如下图:
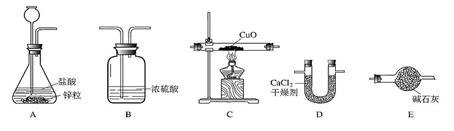
装置的连接顺序为ABCDE,完全反应后,其实验测定的数据如下表所列:
| 实验前 | 实验后 | ||
| C(氧化铜+玻璃管)的质量/g | 75.6 | 69.2 | O元素的质量6.4g |
| D(氯化钙+U型管)的质量/g | 110.8 | 118.0 | H2O的质量 7.2g |
(1)装置A中发生反应的化学方程式为 ,装置B的作用是 。
(2)装置C中的现象为 。
(3)根据实验数据填空:水中氢、氧两种元素的质量比为 。
(4)装置E中碱石灰能吸收水蒸气,若不安装E装置,会使结果中氢元素的质量 ,(填“偏大”“偏小”“不受影响”之一)试简述判断依据 。
(1)Zn+2HCl==ZnCl2+H2 ↑ 吸收A中会发出的水蒸气
(2)黑色粉末逐渐变为红色
(3)1:8
(4)偏大; 空气中的水蒸气会进入D装置,使测得水的质量增大导致计算出H元素的质量增大。(解释合理即可)
(1)装置A中锌与稀盐酸反应生成ZnCl2和H2,故方程式为Zn+2HCl==ZnCl2+H2↑ , 装置B内的浓硫酸常做干燥剂,吸收A中会发出的水蒸气;
(2)装置C中氢气还原氧化铜,黑色氧化铜转变为红色的铜;
(3)由实验数据可知,水中氢、氧两元素的质量比为(7.2g-6.4g):6.4g=1:8;
(4)若不安装装置E则会:空气中的水蒸气会进入D装置,使测得水的质量增大导致计算出H元素的质量增大。