(6分)某实验小组利用图1所示仪器进行“配制一定质量分数的氯化钠溶液”的实验: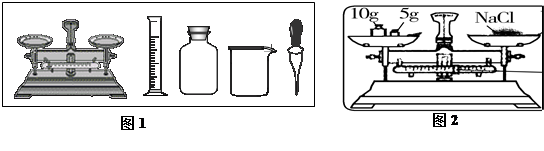
(1)完成此实验正确的操作顺序是 (填序号)。
①溶解 ②把配好的溶液装入试剂瓶 ③称量 ④计算
(2)按实验要求,图1中还缺少的玻璃仪器是 (填名称);氯化钠固体在水中的溶解速度较慢,请写出一种加快氯化钠固体溶解速度的措施: ;如果仪器a中有少量水,就直接倒入氯化钠固体进行溶解,则所配制的氯化钠溶液的质量分数
(填“偏大”、“偏小”或“无影响”)。
(3)小原按图2的操作称取氯化钠,小民发现小原的操作有错误。你认为小原操作中的错误是 。
(4)小民取少量所配制的溶液于试管中,向其中滴入2滴石蕊试液,则溶液的颜色为 。
(1)④③①②(2)玻璃棒 搅拌、加热或减小颗粒大小 偏小 (3)称量时砝码和氯化钠的位置放反了(4)紫色
:(1)配制溶液的步骤是计算、称量、溶解、装瓶;
(2)配制溶液需要的玻璃仪器有烧杯、量筒、滴管、玻璃棒;加快氯化钠固体溶解速度可以搅拌、加热或减小颗粒大小;溶质质量正确,溶剂的质量增加,则溶液的质量增加,故溶质的质量分数偏小;
(3)天平称量物质的质量时应左物右码,图中放反了;
(4)石蕊试液在中性溶液中不变色,氯化钠溶液显中性;