(7分)松花皮蛋是我们喜爱的食品。某小组同学查阅资料得知,制皮蛋料泥的原料主要是:生石灰、纯碱、草木灰(含K2CO3)等。同学们对料泥进行了如下探究:
【猜想】猜想I:料泥的主要成份是Ca(OH)2、NaOH、KOH、CaCO3、灰份;
猜想Ⅱ:料泥的主要成份是NaOH、KOH、Na2CO3、CaCO3、灰份;
猜想Ⅲ:……
【实验与现象】实验过程与现象如下图:
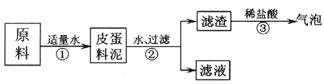
【问题与讨论】
(1)步骤②中,过滤所需要的玻璃仪器有烧杯、玻璃棒、 。
(2)步骤③的现象说明滤渣中含有 (写化学式)。
(3)请写出步骤①中发生反应的化学方程式___。
(4)请设计实验证明滤液的主要成分,并分析猜想Ⅰ或Ⅱ哪个猜想正确。
| 实验步骤 | 实验现象 | 结论和化学方程式 |
(1)漏斗
(2) CaCO3
(3)CaO+H2O==Ca(OH)2, Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
K2CO3+ Ca(OH)2=CaCO3↓+2KOH (写对2个化学方程式给1分)
(4)(若假设Ⅱ成立,操作步骤、实验现象、结论对应正确给分)
| 实验步骤 | 实验现象 | 结论和化学方程式 |
| 取滤液分别放在三支试管中, 第一支试管中滴入足量稀盐酸 第二支试管中滴入酚酞溶液; 第三支试管中通入二氧化碳 | 无明显现象 酚酞溶液变红色 滤液出现白色浑浊 | 滤液中无Na2CO3,但显碱性,滤液中有氢氧化钙 CO2+Ca(OH)2=CaCO3↓+ H2O 2HCl+Ca(OH)2=CaCl2+2H2O 假设I成立(或合理) |
题目分析:(1)过滤需要使用的仪器有:铁架台、漏斗、烧杯和玻璃棒;
(2)步骤③滴加盐酸观察到有气泡产生,结合猜想,滤渣中含碳酸盐,可判断滤渣中一定含有碳酸钙沉淀;
(3)原料中的生石灰与水反应生成氢氧化钙;氢氧化钙与纯碱、草木灰发生反应,生成碳酸钙沉淀和氢氧化钠、氢氧化钾;故化学反应方程式为CaO+H2O==Ca(OH)2, Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,K2CO3+ Ca(OH)2=CaCO3↓+2KOH。
(4)根据题目提供的信息可知,制皮蛋料泥的原料主要是生石灰、纯碱、草木灰(含K2CO3)等,加入适量的水,生石灰和水反应生成熟石灰,氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,过滤得到碳酸钙,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳;可取滤液并加入稀盐酸,如无明显现象,说明滤液中没有碳酸根离子,即猜想Ⅰ正确。
(5)结合以上结论可知,最终产物呈碱性,故无法确定NaOH、KOH中的哪一种或两种的存在。32-检验方法),常用仪器的名称和选用,生石灰的性质与用途,化学式的书写及意义,书写化学方程式
点评:本题属于实验探究题,有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;解答本题时,要根据题目提供的信息,结合实验探究的一般步骤和酸碱盐的性质等知识来解决。
