(12分)(1)小云从电视新闻中了解到:国家新版《生活饮用水卫生标准》已从今年7月1日起强制实施,其中饮用水消毒剂除了目前采用的液氯以外,补充了——氯胺(NH2Cl)、臭氧(O3)。
①O3中氧元素的化合价是 。
②NH2Cl由 (填数字)种元素组成,其中氮元素与氢元素的质量比是 。
③NH2Cl用消毒时,发生反应NH2Cl+X==NH3+HClO,其中X的化学式是 。
(2)小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是他对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下 * * 组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| Ⅰ | 1.2g | ||
| Ⅱ | 1.2g | CuO 0.5g | |
| Ⅲ | 1.2g | MnO2 0.5g |
②若实验Ⅱ比实验Ⅰ的“待测数据”更 (填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
③将实验Ⅱ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将黑色粉末放入试管中, 。(简述操作和现象)
【预期结论】氧化铜还能作氯酸钾的催化剂。
【评价设计】你认为小雨设计实验Ⅲ和实验Ⅱ对比的目的是 。
(3)小雪用如下图所示装置制取氧气的相关数据如下表。回答有关问题:
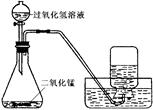
| 气体发生装置内物质的总质量 | |
| 反应前 | 35.6g |
| 反应后 | 34.8g |
②计算参加反应的过氧化氢的质量,写出必要的计算过程。
(1)①0 ②三; 7:1 ③H2O
(2)【设计实验】①所需时间 ②小
③向其中加入适量氯酸钾加热并用带火星的木条放在试管口,观察到木条迅速复燃(合理即可)
【评价设计】探究氧化铜是否比二氧化锰的催化效果好
(3)①0.8 ②1.7g
题目分析:(1)①O3为单质,氧元素的化合价为零;
②由化学式可知,NH2Cl是由氮、氢、氯3种元素组成的,其中氮元素与氢元素的质量比为14:1×2=7:1;
③根据质量守恒定律可知,反应前后原子的种类、数目保持不变,所以反应后NH3和HClO共有1个氮原子、4个氢原子、1个氯原子和1个氧原子,而反应前NH2Cl已有1个氮原子、2个氢原子和1个氯原子,故X应含有2个氢原子和1个氧原子,化学式为H2O。
(2)【设计实验】①该实验的目的是比较氧化铜与二氧化锰二者对过氧化氢分解的催化作用效果的哪个更好,小雨以生成等体积的氧气为标准,考虑因素应为反应所需的时间;
②氧化铜能加快氯酸钾的分解速率,实验Ⅱ比实验Ⅰ所需时间自然更小;
③氧化铜在该反应中起催化剂,反应前后质量与性质都不变,故向其中加入适量氯酸钾加热并用带火星的木条放在试管口,观察到木条迅速复燃;
【评价设计】小雨设计实验Ⅲ和实验Ⅱ对比的目的是比较氧化铜与二氧化锰的哪一个催化效果好。
(3)①根据质量守恒定律和化学方程式2H2O2 2H2O+O2↑可知,氧气的质量=35.6g-34.8g=0.8g;
2H2O+O2↑可知,氧气的质量=35.6g-34.8g=0.8g;
②设参加反应的过氧化氢的质量为X,则
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
X 0.8g
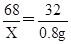 解,得X=1.7g。
解,得X=1.7g。
答:参加反应的过氧化氢的质量为1.7g。
点评:该题为综合性试题,考查知识点较多,应利用已学知识进行逐步分析。
