(9分)已知木炭粉与某红棕色粉末在高温下反应生成二氧化碳和铁。某同学设计了一个实验,证明红棕色粉末中含有氧元素,并测定其中氧元素的质量分数,装置如下图所示。
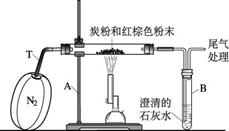
(1)实验前,首先要进行的操作是________________________________________;
(2)实验中,盛放澄清石灰水的大试管中出现的现象是_________________________;
(3)实验中通入纯净而干燥的氮气,其目的是_________________________________;
(4)尾气中可能含有的一种有毒气体是 ;
(5)如果3.2 g该红棕色粉末与碳充分反应,测得澄清石灰水增重1.32 g,则该红棕色粉末中氧元素的质量分数为(5分)写出计算过程如下:
①先检测装置的气密性
②澄清石灰水变浑浊
③将装置中的二氧化碳全部赶入石灰水中
④一氧化碳
⑤略
题目分析:炭粉可以在高温条件下与氧化铁反应,生成二氧化碳与铁;二氧化碳能是澄清石灰水变浑浊。要测定红棕色粉末中含有氧元素,必须保证装置气密性良好,且反应生成的二氧化碳要全部被石灰水吸收才行。故有:
1、实验前,首先要进行的操作是检测装置的气密性;
2、实验中,盛放澄清石灰水的大试管中出现的现象是澄清石灰水变浑浊;
3、实验中通入纯净而干燥的氮气,其目的是将装置中的二氧化碳全部赶入石灰水中;
4、尾气中可能含有的一种有毒气体是一氧化碳;
5、由题意可知,澄清石灰水增重部分应为反应生成二氧化碳的质量,二氧化碳中的氧元素就是从红棕色粉末中得来的。则:
二氧化碳中氧元素的质量为:1.32g×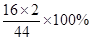 =0.96g
=0.96g
故,红棕色粉末中氧元素的质量分数为: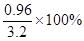 =30%。
=30%。
点评:某元素的质量分数=