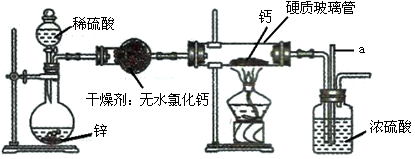
(8分)氢化钙(CaH2)是一种储氢材料,是登山运动员常用的能源提供剂。甲、乙两位同学选用如下装置,用氢气与金属钙加热制备氢化钙。实验结束后,两位同学对硬质玻璃管中的固体进行如下探究:
【提出问题】硬质玻璃管中的Ca是否完全转化为CaH2?
【查阅资料】
① 金属钙活动性很强,遇水反应生成氢氧化钙,同时产生一种气体;
② 氢化钙要密封保存,遇水反应放出氢气。
【猜想与实验】
1、固体为Ca和CaH2。
2、固体为CaH2。
甲同学的探究活动如下:
| 实验操作 | 实验现象 | 实验结论及解释 |
| ① 取少量硬质玻璃管中的固体于试管中,滴入少量的水,收集产生的气体,并用燃着的木条点燃 |
| 有氢气生成 |
| ② 继续向溶液中滴加酚酞 | 呈红色 | 生成 (填化学式) |
【实验反思】
乙同学认为由以上探究活动还不能得出猜想1正确,理由是 。请你帮助乙设计实验,写出主要的实验步骤、现象和相应的结论:
。
【反思讨论】
(1)写出CaH2与水反应的化学方程式 。
(2)登山运动员常用氢化钙固体作能源提供剂,与氢气相比,其优点是 。
(3)制备CaH2装置中,玻璃管a的作用是 。
甲同学的探究活动如下:
| 实验现象 | 实验结论及解释 |
| 冒气泡;气体燃烧,产生淡蓝色火焰 | |
| Ca(OH)2 |
理由是若固体为CaH2,遇水反应也会产生相同的现象。
主要的实验步骤、现象和相应的结论:
取等质量的氢化钙和待测固体,分别放入两支试管中,加入足量的水,使其充分反应,收集产生的气体,比较反应产生气体的体积。若体积相等,说明玻璃管中Ca完全转化为CaH2;若不相等,则说明Ca未完全转化为CaH2。
【反思讨论】
(1) CaH2 +2H2O Ca(OH)2 + 2H2↑。
(2) 便于携带、避免爆炸危险。
(3) 检验装置的气密性。
题目分析:【猜想与实验】
| 实验操作 | 实验现象 | 实验结论及解释 |
| ① 取少量硬质玻璃管中的固体于试管中,滴入少量的水,收集产生的气体,并用燃着的木条点燃 | 冒气泡;气体燃烧,产生淡蓝色火焰 | 有氢气生成 |
| ② 继续向溶液中滴加酚酞 | 呈红色 | 生成Ca(OH)2(填化学式) |
【反思讨论】
(1)CaH2与水反应的化学方程式为CaH2 +2H2O Ca(OH)2 + 2H2↑。
(2)登山运动员用氢化钙固体作能源提供剂,与氢气相比,其优点是便于携带、避免爆炸危险。
(3)制备气体的装置不能漏气,故制备CaH2装置中,玻璃管a的作用是检验装置的气密性。
点评:根据题中给定的信息,分析实验装置和所用药品的性质,根据装置和药品性质来设计实验,才能得到探究的结果。书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
