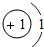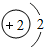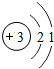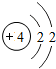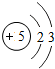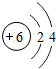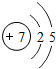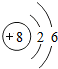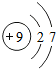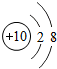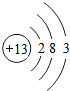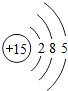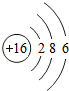问题
问答题
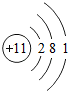
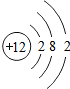
元素周期表是化学学习的重要工具,依据下表回答问题:
| 第一周期 | 1H
| 2He
| ||||||
| 第二周期 | 3Li
| 4Be
| 5B
| 6C
| 7N
| 8O
| 9F
| 10Ne
|
| 第三周期 | 11Na
| 12Mg
| 13Al
| 14Si
| 15P
| 16S
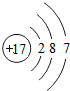
| 17Cl
| 18Ar
|
(2)通过上表的分析可知:元素所在的周期数=______,元素所在的族数=该元素原子的最外层电子数.
(3)根据上表中原子核外电子排布规律,原子序数为19的钾元素的原子结构示意图为______,钾元素的原子在化学反应中容易形成离子,该离子符号是______.
答案
(1)14号元素是硅,硅元素带石字旁,是非金属元素;最外层电子数决定元素的化学性质,最外层电子数相同的元素,化学性质相似,硅元素原子最外层电子数为4,碳元素原子最外层电子数为4,因此硅、碳元素的化学性质相似,常温下也具有稳定性;
故答案为:非金属;碳;稳定;
(2)通过上表的分析可知:元素所在的周期数=元素原子的电子层数,元素所在的族数=该元素原子的最外层电子数;
故答案为:该元素原子核外的电子层数;
(3)根据上表中原子核外电子排布规律,原子序数为19的钾元素在第四周期、第一主族,应有4个电子层,最外层电子数是1,因此钾原子结构示意图为
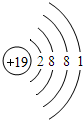
;钾元素的原子最外层有一个电子,在化学反应中容易失去1个电子形成氧离子,该离子符号是K+.
故答案为:
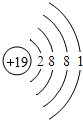
;K+.