元素周期表是化学和研究化学的重要工具,它的内容十分丰富,下图是依据元素周期表画出的1~18号元素的原子结构示意图.请对它进行探究
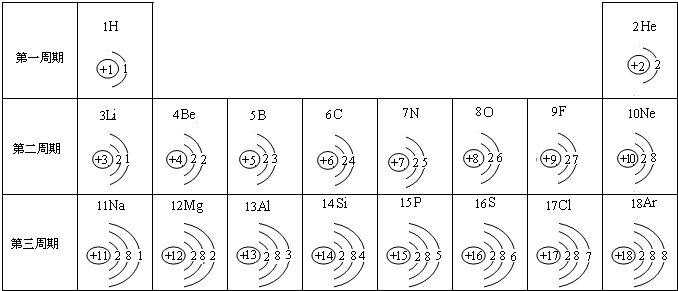
(1)原子序数为17的元素名称是______,在化学反应中,该元素的原子容易______(填“得”或“失”)电子;原子序数为13的元素属于______元素(填“金属”或“非金属”).
(2)请从上表中总结出一条原子排布的规律______.
(3)研究表明:第二周期从3号到9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力增大,故原子半径逐渐减小.请判断:钠原子半径______镁原子半径(填“<”或“>”或“﹦”).
(1)根据金属元素的原子最外层电子数一般少于4个,可知原子序数为13的元素属于金属元素;非金属元素的原子最外层电子数一般多于4个,可知原子序数为17的元素为非金属元素,名称是氯;非金属元素在化学反应中易得到电子,形成阴离子;
(2)从上表中总结出规律有:①原子最外层电子数一般不超过8个;(或金属元素的原子最外层电子数一般少于4个,非金属元素的原子最外层电子数一般多于4个)
(3)钠和镁的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力增大,故原子半径逐渐减小.
故答案为:(1)氯元素;得;金属;
(2)每一横行电子层数相等;或每一横行最外层电子数依次增加;或每一纵行最外层电子数相同;或每一纵行最外层电子数依次增加…;
(3)>.
