某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为 .
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的 和 都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |
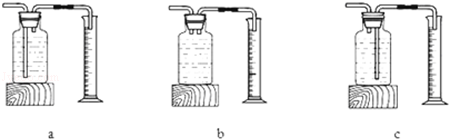
①若用上述装置测生成氧气的体积,则用图 (填“a”“b”或“c”)
②实验结论:在相同条件下, ,双氧水分解得快.
(1)Ⅰ、3.0;
Ⅱ、质量;化学性质;
(2)①c;
②双氧水浓度越大.
题目分析:(1)Ⅰ、根据控制双氧水的质量和质量分数相等才能比较出二氧化锰和氧化铜的催化效果分析.
Ⅱ、根据催化剂的定义进行解答;
(2)①根据气体短管进长管出才能排出试剂瓶中的水、表中实验数据和生成氧气可以知道:敞口的容器中剩余物质的质量减轻分析.
②实验结论:根据题干中表格中所给的数据进行分析并完成解答.
解:(1)Ⅰ、控制双氧水的质量和质量分数相等才能比较出二氧化锰和氧化铜的催化效果,所以也应该取3.0g过氧化氢溶液;
Ⅱ、根据催化剂的定义可以知道,要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的质量和化学性质都没有改变;
(2)①气体短管进长管出才能排出试剂瓶中的水,所以应该选择c装置作为实验装置;
②实验结论:从表中实验数据可知双氧水浓度越大,分解得越快.
故答案为:(1)Ⅰ、3.0;
Ⅱ、质量;化学性质;
(2)①c;
②双氧水浓度越大.
点评:本题通过实验探究了二氧化锰和氧化铜在过氧化氢制氧气中的催化作用,侧重实验能力和分析能力的考查.
