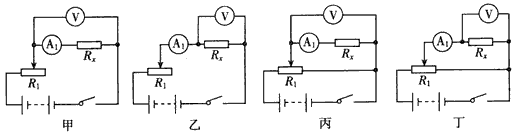
下面是某兴趣小组同学做的3个小实验。根据实验内容回答下列问题(仪器的固定装置已经省略)。
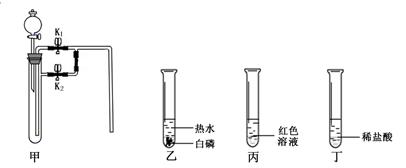
(1)若甲中为二氧化锰,连接甲乙装置,______________(填开关“K1”和“K2”的操作),从分液漏斗向甲中加入适量双氧水,该实验可以证明可燃物燃烧需要与氧气接触。甲中发生反应的化学方程式为____________________。
(2)若甲中为水,丙中为红色溶液,连接甲丙,打开K1,关闭K2,从分液漏斗向甲中加入某药品后,丙中只看到溶液由红色变为无色。写出丙中发生反应的化学方程式______。
(3)若甲中为二氧化碳(K1、K2关闭),连接甲丁,从分液漏斗向甲中加入适量的澄清石灰水,一段时间后,打开K1,整个实验过程中甲中观察到现象是______________________。
MnO2 |
 2H2O2 2H2O + O2↑
2H2O2 2H2O + O2↑(2)2NaOH + H2SO4 = Na2SO4 + 2H2O
(3)澄清石灰水变浑浊,打开K1后,丁中液体倒吸入甲,产生无色气泡,浑浊减少(消失),甲中液体流入丁。
题目分析:(1)双氧水在二氧化锰的催化作用下分解,生成水和氧气,故反应的化学方程式为2H2O2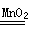 2H2O + O2↑;由于在双氧水加入后,下端的导气管口会被液封,且气体的密度都较小,会从上面的管口逸出,故需关闭K1,打开K2。
2H2O + O2↑;由于在双氧水加入后,下端的导气管口会被液封,且气体的密度都较小,会从上面的管口逸出,故需关闭K1,打开K2。
(2)根据“只看到丙中溶液由红色变为无色”,说明丙中溶液原为滴有酚酞的碱液,遇到了来自于甲中的酸,酸中和了丙中的碱,故酚酞变为无色,且该酸碱中和反应无其他现象;再根据题意,“连接甲丙,打开K1,关闭K2,从分液漏斗向甲中加入某药品后,丙中只看到溶液由红色变为无色”,说明甲中的酸是在气压的作用下,从下端的导气管口进入丙的,而甲中原有水,由此可知,从分液漏斗向甲中加入的是浓硫酸,遇水放热使甲中气体膨胀,压强增大,从而将硫酸压入丙,与其中的碱液反应,如2NaOH + H2SO4 = Na2SO4 + 2H2O。
(3)若甲中为二氧化碳(K1、K2关闭),连接甲丁,从分液漏斗向甲中加入适量的澄清石灰水,二者反应生成碳酸钙沉淀,故可见澄清石灰水变浑浊;一段时间后,打开K1,由于甲中气体减少,压强减小,故在大气压的作用下,丁中稀盐酸会被倒吸入甲,与之前反应生成的碳酸钙沉淀反应,生成氯化钙、水和二氧化碳气体,故可见有无色气泡产生,浑浊减少。
点评:对于验证型实验探究,要熟记物质的性质或变化规律,根据给出的实验设计方案,进行实验、分析和探究,并通过观察、记录和分析的实验现象,来验证该物质的性质或变化规律等。