某同学将光亮的镁条放入滴有酚酞的NaHCO3饱和溶液中,产生大量气泡和白色固体,溶液红色加深.
(一)溶液红色加深,则反应后溶液的碱性 (填“增强”、“不变”或“减弱”).
(二)为确定气体和固体的成分,该同学进行了如下的探究.
(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为 (写化学式).
(2)对白色固体做出如下猜测并进行实验:
【猜测】
查阅资料1:Mg(HCO3)2能溶于水.
①白色固体可能是MgCO3;
②白色固体可能是 ;
③白色固体可能是MgCO3和Mg(OH)2.
【实验】
①取洗净后的白色固体,加入足量的 溶液,观察到 ,则白色固体一定含有MgCO3.
查阅资料2:MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物.
②为进一步确定白色固体的组成,该同学进行了定量实验:
称取干燥的白色固体22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,浓硫酸增重1.8g,则白色固体中含有 ,再通过碱石灰,碱石灰增重8.8g,则固体中各成分的质量比为 .
(一)增强
(二)(1)H2 (2)Mg(OH)2.
【实验】
①稀盐酸;有气泡产生
②Mg(OH)2 84:29或29:84
题目分析:(一)溶液红色加深,则反应后溶液的碱性增强.
故填:增强.
(二)(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为氢气,氢气的化学式是H2.
故填:H2.
(2)白色固体可能是MgCO3,白色固体可能是Mg(OH)2,白色固体可能是MgCO3和Mg(OH)2.
故填:Mg(OH)2.
【实验】
①取洗净后的白色固体,加入足量的稀盐酸溶液,观察到有气泡产生,则白色固体一定含有MgCO3.
故填:稀盐酸;有气泡产生.
②碳酸镁受热分解生成氧化镁和二氧化碳,氢氧化镁受热分解生成氧化镁和水,分解产生的气体全部先通过浓硫酸,浓硫酸增重1.8g,说明白色固体中含有氢氧化镁,分解生成水的质量是1.8g.
故填:Mg(OH)2.
解:设氢氧化镁的质量为X,
Mg(OH)2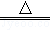 MgO+H2O,
MgO+H2O,
58 18
X 1.8g
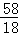 =
=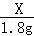 ,
,
X=5.8g,
则碳酸镁的质量为:22.6g﹣5.8g=16.8g,
氢氧化镁和碳酸镁的质量比为:5.8g:16.8g=29:84,那么碳酸镁和氢氧化镁的质量比为84:29.
故填:84:29或29:84.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.
