利用下图装置可进行气体性质的探究实验。A处通入无色气体(可能是H2、CO或CO2);
B处玻璃管中盛放黑色粉末(可能是CuO或C),C处试管中盛放澄清石灰水。

(1)根据要求完成下表填写:
| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象: 。 |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式: , 发生氧化反应的物质是: 。 |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有 色的火焰。 |
(2)探究实验Ⅰ通过B处的现象只能确定一种产物是铜,为了进一步确定另一产物是水,请对上述实验装置提出简要修改方案(添加或更换装置的位置和所需的药品) 。
(3)探究实验Ⅱ澄清石灰水的作用(用发生反应的化学方程式表示) 。
(4)在上述探究实验Ⅱ、Ⅲ中,D处导管尖嘴口都需用酒精灯点燃,简述其目的分别是: 、 。
(1)黑色粉末变成红色(玻璃管内壁有水珠)
CO+ CuO Cu + CO2 )CO 蓝
Cu + CO2 )CO 蓝
(2)位置:在B、C之间或C之前; 药品:白色无水硫酸铜或C装置更换盛有白色无水硫酸铜的干燥管
(3)CO2+Ca(OH)2→CaCO3↓+ H2O
(4)实验Ⅱ目的是除去有毒的CO尾气,防止污染 实验Ⅲ主要目的是证明高温下CO2与C能反应,且产物为CO
试题解析:H2还原CuO的反应现象是:黑色粉末变成红色,玻璃管内壁有水珠,CO+ CuO Cu + CO2
Cu + CO2
在氧化还原反应中,含氧化合物里的氧被夺去的反应,叫还原反应。物质跟氧发生的反应,叫氧化反应。CO被氧化铜氧化,发生氧化反应。CO2与C 的反应后可生成CO,CO燃烧产生蓝色火焰。
H2还原CuO后生成铜和水,白色硫酸铜遇水变蓝,可用来鉴别水的生成,因此可在B、C之间或C之前安装盛有无水硫酸铜的干燥管。(15)澄清石灰水可鉴别二氧化碳,化学方程式为:CO2+Ca(OH)2→CaCO3↓+ H2O
CO有毒,可用点燃的酒精灯除去的尾气中的CO,防止污染空气。
高温下CO2与C能反应,且产物为CO

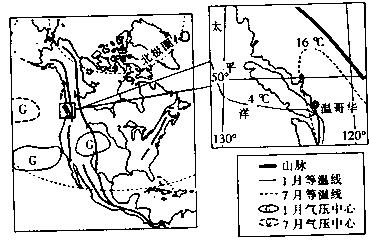
 种气候类型,其中代表温哥华气候类型的是
种气候类型,其中代表温哥华气候类型的是 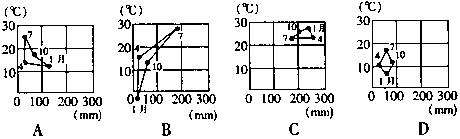
 区冬、夏季主导风向的成因。
区冬、夏季主导风向的成因。