(4分)海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。下图是某厂生产纯碱的工艺流程图:
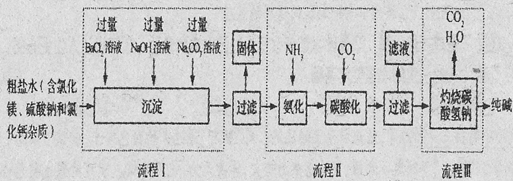
请完成下列问题:
(1)该厂最终产品有 (填物质名称);
(2)流程Ⅰ中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是
(填字母序号)
A.加入三种物质的顺序不能调整
B.加入三种溶液将粗盐水中的SO42-、Mg2+、Ca2+转化为沉淀
C.按流程Ⅰ所加溶液的顺序除杂,过滤后得4种沉淀
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化铵,氨气在制碱过程中的作用
是 ;
(4)写出Ⅲ中发生反应的化学方程式 。
(1)碳酸钠和氯化铵。(2)BC
(3)可增加二氧化碳吸收量
(4)2NaHCO3△Na2CO3+H2O+CO2↑
题目分析:(1)流程Ⅱ可生成碳酸氢钠和氯化铵,氯化铵可作氮肥。碳酸氢钠在流程III中会生成碳酸钠。所以该厂最终的产品有碳酸钠和氯化铵。
(2)加入氯化钡可与硫酸根离子结合形成硫酸钡沉淀;加入氢氧化钠是为了除去镁离子;加入碳酸钠是为了除去钙离子。所以B项正确。为了完全除去硫酸根离子,所以需要加入过量的氯化钡。而钡离子有毒,需要让过量的钡离子形成沉淀,而加入的碳酸钠即可与钡离子结合形成碳酸钡沉淀。所以按图示加入的顺序 * * 生四种沉淀。C项正确。根据上述分析可知加入碳酸钠一定要在加入氯化钡之后,其它顺序可以调整。所以A项不正确。所以应选BC项。
(3)将氯化钠转化为碳酸钠需要形成碳酸根,所以应吸收大量的二氧化碳。而氨气的水溶液呈碱性,可增加二氧化碳吸收量。
(4)流程III中,碳酸氢钠在加热的情况下生成碳酸钠、水和二氧化碳。反应的化学方程式为:2NaHCO3△Na2CO3+H2O+CO2↑