通过化学学习,你已经掌握了实验室制取气体的有关规律.如图是某研究性学习小组设计的几种装置,请分析并回答下列问题:
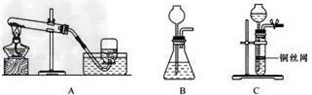
(1)用A装置可制取的气体是_________,化学反应方程式为_________.
(2)B、C两装置都可用作实验室制取O2、H2的发生装置,写出用此两装置制取其中一种气体的化学方程式_________.
(3)C装置是在B装置基础上增加隔离铜丝网改进而来的,它的优点是_________.在实验室制取CO2时,若隔离网改用铝丝做成,那么产生的后果是_________,其原因是_________(写化学方程式).
(4)实验室制取二氧化碳一般有以下步骤:①检查装置的气密性;②按要求连接制取装置;③向长颈漏斗中注入盐酸;④收集气体;⑤向大试管内放入石灰石,操作顺序正确的是_________
A.①②③④⑤B.②①③④⑤C.②①⑤③④D.③④⑤②①
(5)气体的收集方法取决于气体的_________.
(6)小明采用C装置制取二氧化碳,称取12g石灰石,加入足量的稀盐酸,充分反应后,共收集到二氧化碳4.4g(假设生成的气体全部收集),试计算该石灰石中碳酸钙的质量分数.(计算结果保留到小数点后一位)
(1)氧气;2KClO3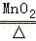 2KCl+3O2↑
2KCl+3O2↑
(2)2H2O2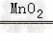 2H2O+O2↑;
2H2O+O2↑;
(3)可随时控制反应的发生和停止;制得的气体不纯;2Al+6HCl==2AlCl3+3H2↑;
(4)C;
(5)气体的密度和溶解性;
(6)设CaCO3的质量为x.
CaCO3+2HCl==CaCl2+CO2↑+H2O
100 44
x 4.4g
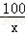 =
=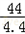
解之得:x=10g
该石灰石样品中碳酸钙的质量分数为: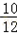 ×100%=83.3%
×100%=83.3%
答:石灰石中碳酸钙的质量分数为83.3%.
