为制取并收集一瓶干燥的CO2气体,某课外研究小组向实验教师领取了下列仪器和药品:
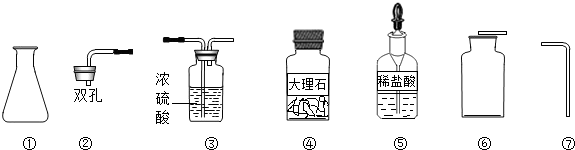
(1)写出编号仪器的名称①______;⑥______.要完成该实验,他们还必须向实验老师领取的仪器有镊子、火柴和______.
(2)实验室制取CO2时发生反应的化学方程式为______.
(3)收集CO2时,他们如何检验CO2已收集满?______;
(4)本实验的装置也可以用来制取我们所熟悉的一种气体是______;
(5)实验室制取气体要选择适当反应物.我们知道实验室制取大量CO2气体不能用浓盐酸和大理石为原料,因为______;也不能用稀硫酸和大理石为原料,因为______.他们对实验室制取CO2的实验条件展开了进一步的探究,做了如下四个对比实验:
①取m g大理石粉末与足量的溶质质量分数为5%的盐酸反应;
②取m g块状大理石与足量的溶质质量分数为5%的盐酸反应;
③取m g大理石粉末与足量的溶质质量分数为10%的盐酸反应;
④取m g块状大理石与足量的溶质质量分数为10%的盐酸反应.
实验现象:产生气泡的快慢顺序为③>①>④>②.
实验结论:影响大理石和盐酸反应产生CO2快慢的因素有______.
(1)仪器的名称①锥形瓶;⑥集气瓶.因为要制取干燥的二氧化碳气体,他们还必须向实验老师领取的仪器是 洗气瓶.
(2)实验室制取CO2时发生反应的化学方程式为 2HCl+CaCO3=CaCl2+H2O+CO2↑.
(3)因为二氧化碳密度大,收集CO2时,检满的方法是 把燃着的火柴平放到集气瓶口,火柴若熄灭,证明已收集满二氧化碳;
(4)本实验的装置也可以用来制取我们所熟悉的一种气体是 氧气;因为氧气也可以用过氧化氢溶液通过固体+液体→气体制的.
(5)实验室制取大量CO2气体不能用浓盐酸和大理石为原料,因为 浓盐酸易挥发出氯化氢气体,会使收集的CO2不纯;也不能用稀硫酸和大理石为原料,因为 稀硫酸和大理石反应生成CaSO4微溶于水,会阻碍反应的继续进行.通过对比实验,可得出结论:影响大理石和盐酸反应产生CO2快慢的因素有 大理石与盐酸的接触面积和盐酸的溶质质量分数.
答案:(1)①锥形瓶;⑥集气瓶;洗气瓶
(2)2HCl+CaCO3=CaCl2+H2O+CO2↑
(3)把燃着的火柴平放到集气瓶口,火柴若熄灭,证明已收集满二氧化碳
(4)O2
(5)浓盐酸易挥发,会使收集的CO2不纯.稀硫酸和大理石反应生成CaSO4不溶于水,会阻碍反应的继续进行.因素有大理石与盐酸的接触面积和盐酸的溶质质量分数.

