(14分)由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀。两电极的材料分别为石墨和铁。
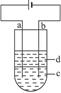
(1)a电极材料应为________________________________________,电极反应式为
_______________________________________________________;
(2)电解液c可以是(填编号)( )
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为______________________________________________________,在加入苯之前对c应作怎样的简单处理?
______________________________________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)( )
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为________________________________。
(1)Fe Fe-2e-====Fe2+
(2)BC
(3)隔绝空气,防止Fe(OH)2被空气氧化 加热一段时间
(4)BC
(5)白色沉淀立即变为灰绿色,最终变为红褐色
要想制得Fe(OH)2,必须有Fe2+和OH-,所以铁必须作阳极,本身溶解成Fe2+。电解质溶液电解后,应存在大量的OH-,NaCl溶液电解,阴极H+放电后,产生了OH-,NaOH溶液电解,实际上电解了H2O,也有OH-。为了防止Fe(OH)2被氧化,要隔绝空气,并把溶液中的氧气赶走。为了快速产生白色沉淀,要加快反应速率,并使得两电极间距离适当减少。反接电源电解,原阴极4OH--4e-====O2↑+2H2O,产生氧气会把Fe(OH)2氧化成Fe(OH)3。
