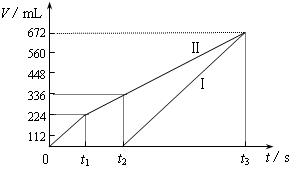
常温下用惰性电极电解200 mL 一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(以下气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
⑴通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度;
②t2时所得溶液的pH;
⑵若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中的氯离子浓度的取值范围为 ,铜离子浓度的取值范围为 。
⑴①阳极首先逸出的是Cl2
n(NaCl)=2n(Cl2)=0.02 mol,则c(NaCl)=0.1mol/L (1分)
阳极得到336 mL气体中,含0.01 mol Cl2和0.005 mol O2
转移电子的物质的量为:0.01 mol×2+0.005 mol×4=0.04 mol
此过程中阴极刚好全部析出铜
n(CuSO4)=n(Cu)=0.04 mol÷2=0.02 mol
则c(CuSO4)=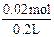 =0.1mol/L (2分)
=0.1mol/L (2分)
②t2时溶液中c(Na+)=0.1 mol/L,c(SO42-)=0.1 mol/L
根据电荷守恒有:c(H+)=2×0.1 mol/L-0.1 mol/L=0.1 mol/L
即溶液的pH=1 (2分)
⑵0<c(Cl-)<0.1mol/L(2分) 0<c(Cu2+)<0.05mol/L(2分)
