问题
选择题
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液, 恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为[ ]
A.(b-a)/V mol/L
B.(2b-a)/V mol/L
C.2(b-a)/V mol/L
D.2(2b-a)/V mol/L
答案
答案:D
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液, 恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为[ ]
A.(b-a)/V mol/L
B.(2b-a)/V mol/L
C.2(b-a)/V mol/L
D.2(2b-a)/V mol/L
答案:D
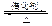 2SO3(g)。
2SO3(g)。(A)升高温度 (B)降低温度 (C)增大压强
 2SO3(g) ΔH=-197kJ·mol-1。现有甲、乙、丙三个相同的容积不变的容器,按下表中数据充入气体并反应达到平衡,放出或吸收的热量的数值分别为Q1、Q2、Q3。下列说法中不正确的是 。
2SO3(g) ΔH=-197kJ·mol-1。现有甲、乙、丙三个相同的容积不变的容器,按下表中数据充入气体并反应达到平衡,放出或吸收的热量的数值分别为Q1、Q2、Q3。下列说法中不正确的是 。容器 | SO2(mol) | O2(mol) | SO3(mol) | 热量(kJ) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 |
| 0 | Q2 |
丙 | 0 | 0 | 1 | Q3 |
 2 < Q3 < 197kJ
2 < Q3 < 197kJ⑷氨水吸收工业制硫酸尾气中的SO2的化学反应为:
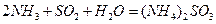

下列措施中能 提高燃煤烟气中
提高燃煤烟气中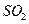 去除率的有 (填字母)。
去除率的有 (填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-