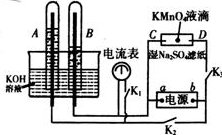
(9分)在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂
夹夹在被Na2SO4溶液浸湿的滤纸条上.滤纸条的中部滴有KMnO4液滴;电源有a、b两极。在A、B 中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3,通直流电。
(1)写出B中电极反应式__________。
(2)在湿的硫酸钠溶液滤纸条中部的高锰酸钾液滴处发生的现象是______________。
(3)电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针________(填。是”或。否”)移动,其理由是_______________________。
(4)在298K,若2g B 气体和0.5mol的A 气体完全反应,生成物为液态,放出
285・8kJ热量,写出此反应的热化学方程式:__________________________________。
(1)2H++2e-=H2 ,(2)紫红色向D处移动:(3)是;形成氢氧原电池
(4)2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ·mol-1
(1)切断K1,闭合K2、K3,通直流电,则构成电解池。B中液面低于A中的,说明B中产生的气体多。因为电解氢氧化钾溶液生成物是氢气和氧气,所以B中产生的是氢气,即B为阴极,则电源的a极是负极。所以C是阴极,D是阳极。
(2)在电解池中阴离子向阳极移动,所以紫红色向D极移动。
(3)切断K2、K3,闭合K1,则此时A和B构成构成氢阳燃料电池,所以电流表的指针发生偏转。
(4)考查热化学方程式的书写。
