(7分)医用氯化钙常用于合成药物。以工业碳酸钙(含少量Fe3+等杂质)为原料生产二水和氯化钙(CaCl2·2H2O)的流程如下图所示。
|
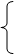
|


 滤渣
滤渣
(1)写出第①步中碳酸钙与盐酸反应的化学方程式:_____________________
(2)第②步中是否发生化学变化?___________(填“是”或“否”)。
(3)操作a的名称是______________,实验室进行该操作时玻璃棒的作用是___________________。
(4)青少年正处于生长发育阶段,需要摄入足够的钙,写出一个合理的补钙方法:_____________
______________________________________________________________。
(7分)(1)CaCO3+2HCl==CaCl2+H2O+CO2↑ (2分)
(2)是(1分) (3)过滤 、引流(各1分) (4)多吃富含钙的食物(2分)
分析:(1)根据识记的知识直接写出反应的方程式
(2)判断是不是发生了化学变化,关键是看是否生成了新的物质
(3)根据操作a得到的物质可以判断操作a应该是过滤,进而确定玻璃棒的作用
(4)补钙的方法有多种,建议通过饮食来补钙
解:(1)可以直接写出碳酸钙与盐酸的反应的方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)氢氧化钙要和氯化铁反应生成沉淀,过滤后得到滤渣可以说明这点,故本题答案为:是
(3)最后得到了滤液和滤渣,可以确定操a为过滤,此操作中玻璃棒的作用为引流故本题答案为:过滤 引流
(4)在日常生活中可以多吃一些含钙的食物和蔬菜能够补充人体所需的钙质,故本题答案为:多吃富含钙的食物
点评:本题题主要考查了一些实验基本操作,要知道分离固体和液体的一种常用方法----过滤.同时明确玻璃棒的作用为引流.熟记化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑,熟练掌握碱的化学性质.
