(14分)请根据所学的电化学原理,解决以下问题。
(1)依据氧化还原反应:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s) 设计的双液原电池,可以提供稳定的电流。装置如图所示,其中盐桥中装有琼脂—饱和KCl溶液。
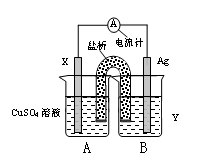
回答下列问题:
①电极X的材料和电解质溶液Y分别为 ;
②盐桥中K+移向 (填A或B);
③银电极发生的电极反应为 。
(2)下图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

①若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液, (填X或Y)电极附近先变红色, X极上的电极反应式为 。
②若要在铁制品上镀一定厚度的Cu层,Y电极反应式为
③若X、Y都是铂电极,电解某金属M的氯化物(MCl2)溶液,当收集到1.12 L氯气时(标准状况),阴极增重3.2 g。该金属的相对原子质量是 ;
( 14分)(每空2分)
(1)①Cu、AgNO3溶液 ②B ③Ag+ + e- = Ag
(2)①X 2H2O +2e-=H2↑+OH-(或2H++ 2e- =H2↑ )
②Cu - 2e- =Cu2+ ③64
(1)①在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。根据总反应式可知,铜失去电子,所以铜是负极,即X是铜。银离子得到电子,所以正极溶液中电解质是硝酸银溶液。
②原电池阳离子向正极移动,即K+移向B。
③银电极是正极,溶液中的银离子得到电子,方程式为Ag+ + e- = Ag。
(2)①惰性电极电解饱和氯化钠溶液,阴极是氢离子放电,从而破坏阴极周围水的电离平衡,所以阴极周围溶液显碱性,溶液显红色。根据装置图可知,X与电源的负极相连,做阴极,所以电极反应式为2H++ 2e- =H2↑ 。
②电镀时,待镀金属作阴极,镀层金属作阳极,含有镀层金属离子的溶液作电解质溶液。根据装置图可知,Y与电源的正极相连,作阳极,所以是铜,电极反应式为Cu - 2e- =Cu2+。
③1.12 L氯气时(标准状况)是0.05mol,转移电子是0.05mol×2=0.1mol,所以根据电子得失守恒可知,金属的相对原子质量是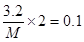 ,解得M=64。
,解得M=64。
