(12分)研究钢铁的腐蚀与防护具有非常重要的意义。
(1)铁的电化学腐蚀包括两种,这两种腐蚀的负极反应均为 ,而正极反应由铁表面的水膜酸碱性决定,当水膜酸度较高时,正极反应式为 ,这种腐蚀称为 腐蚀,而水膜酸性不强时,正极反应式为 ,这种腐蚀称为 腐蚀。
(2)防止钢铁腐蚀的电化学方法有两种,下图中液体为海水,请在图中添加必要的导线、电源,注明另一电极的电极材料名称,使其符合图下所注的保护方法:
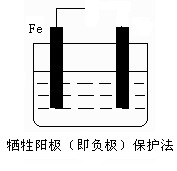

(1)(电极反应式每个2分,其他每个1分)
Fe -2e– =Fe2+ 2H++ 2e– = H2↑ 析氢 O2+2H2O+ 4e– =4OH– 吸氧
(2)(毎图2分)
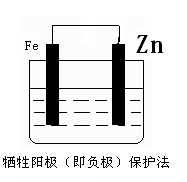
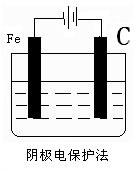
考查金属的腐蚀与防护
(1)金属发生电化学腐蚀,金属均是失去电子,作负极,反应式是Fe -2e– =Fe2+ 。当水膜酸度较高时,发生析氢腐蚀,正极反应式为2H++ 2e– = H2↑;而水膜酸性不强时,则发生吸氧腐蚀,正极反应式为O2+2H2O+ 4e– =4OH–。
(2)电化学防止金属腐蚀的方法有两种,分别是牺牲阳极的阴极保护法和外加电流的阴极保护法。因此左图中需要一种金属性强于铁的,例如锌;而右图中铁应该作阴极,和电源的负极相连,所以正确的图示是

