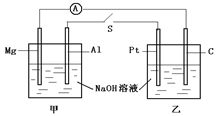
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是
A.电流计指针不发生偏转
B.Al、Pt两电极有氢气生成
C.甲池pH减小,乙池pH不变
D.Mg、C两电极生成的气体在一定条件下可恰好完全反应
答案:D
题目分析:Al是负极,Mg是正极
负极:Al + 4OH- -3e- =AlO2- +2H2O
正极:2H2O + 2e- =H2↑ + 2OH-
总反应式:2Al +2NaOH +H2O = 2NaAlO2+3H2 ↑
Pt是阴极,C是阳极
阳极:4OH- - 4e = 2H2O + O2↑
阴极:2H2O + 2e = H2↑ + 2OH-
总反应式:2H2O = 2H2↑ + O2↑
A、错误。左边是原电池,右边是电解池,电流表指针发生偏转。
B、错误。Al是负极,没有H2;Mg是正极,产生H2
C、错误。乙是电解水,水减少,NaOH浓度增大,pH增大
D、正确。正好产生H2和O2,且体积比是2:1,一定条件下可恰好完全反应。
故选D
点评:注意分析装置的特点,准确判断出原电池(1、有活动性不同的电极,2、有电解质溶液,3、有闭合回路,4、有自发的氧化还原反应。)与电解池(特点:有外接电源)。
